Перелом позвоночника и ревматоидный артрит

Переломы костей скелета у больных ревматоидным артритом возникают в 1,5-2 раза чаще, чем в популяции, являются одной из причин снижения качества жизни, инвалидизации и смерти больных. В настоящем исследовании, включавшем 254 женщины с ревматоидным артритом (диагноз был установлен по критериям Американской коллегии ревматологов) в возрасте от 18 до 85 лет, с давностью заболевания от полугода до 42 лет, сравнивали группу пациенток с переломами и без переломов в анамнезе с целью идентификации факторов рисков переломов при РА. Переломы в анамнезе ассоциировались с приемом глюкокортикостероидов (ГКС), более высокой кумулятивной дозой и более длительным приемом ГКС. Также отмечено, что в группе пациенток с переломами показатели минеральной плотности кости (МПК) были ниже во всех исследуемых участках скелета. На основании проведенного сравнения наиболее вероятными факторами риска переломов у больных ревматоидным артритом являются возраст, длительный прием ГКС в высоких дозах, низкие значения МПК, тяжелое течение ревматоидного артрита и его осложнения.

Таблица 1. Антропометрическая и клинико-рентгенологическая характеристика включенных в исследование пациенток с ревматоидным артритом: группы с переломами и без переломов в анамнезе
Таблица 2. Сравнительная частота выявления остеопороза по показателю МПК в различных отделах скелета в группах больных ревматоидным артритом с переломами и без переломов в анамнезе*
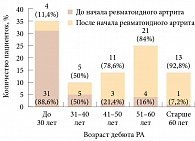
Рисунок. Возникновение первого перелома у больных ревматоидным артритом в зависимости от возраста возникновения перелома и наступления заболевания
Таблица 3. Характеристика больных с переломом шейки бедренной кости
Ревматоидный артрит (РА) – наиболее распространенное аутоиммунное воспалительное заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом (синовитом) и системным поражением внутренних органов. В мире этим заболеванием страдают от 0,5 до 1% людей [1]. Среди наиболее частых социально значимых, жизнеугрожающих осложнений течения и терапии РА рассматриваются сердечно-сосудистые катастрофы, тяжелые инфекции, амилоидоз и переломы различных локализаций, которые, по данным зарубежных авторов, у больных РА возникают в 1,5-2 раза чаще, чем в популяции. Что касается перелома шейки бедра (ШБ), наиболее опасного перелома в отношении дальнейшего прогноза для жизни и трудоспособности, его относительный риск (ОР) достигает 2,1 [2]. По данным финских авторов, этот показатель еще выше – 3,26 [3]. Не менее значимыми причинами снижения качества жизни и инвалидизации являются деформации и переломы позвонков. У больных РА они случаются в 2-4 раза чаще, чем в популяции [4-6].
К наиболее значимым факторам риска переломов у больных РА относятся: снижение минеральной плотности кости (МПК), прием и кумулятивная доза глюкокортикостероидов (ГКС), менопауза, низкий индекс массы тела (ИМТ), склонность к падениям. Однако наибольший интерес представляет вклад самого заболевания и его течения, хронического воспаления и концентрации провоспалительных цитокинов в моделирование и ремоделирование костной ткани, в увеличение риска переломов у больных РА.
Как известно, периартикулярный остеопороз – наиболее ранний признак изменений в костной ткани при РА. Генерализованный остеопороз присоединяется позже. Установлено, что в патогенезе вторичного остеопороза и эрозивно-деструктивных изменений в суставах при РА ключевую роль играют провоспалительные цитокины (фактор некроза опухоли альфа, интерлейкины 6, 1 и др.). Провоспалительные цитокины способны связываться с рецепторами на поверхности остеокластов и запускать процессы костной резорбции. Из-за дисбаланса между костеобразованием и костной резорбцией нарушается минерализация, изменяется структура и микроархитектоника костной ткани, уменьшается плотность кости. Это приводит к возникновению остеопороза, снижению прочности кости, а в конечном итоге – к переломам.
В ряде зарубежных исследований были проанализированы возможные факторы риска (ФР) переломов у больных РА. В некоторых работах использовали небольшие выборки, что повлияло на репрезентативность полученных результатов [7, 8]. В одних исследованиях изучались конкретные локализации переломов (только вертебральные [1, 4, 7, 9] или, напротив, вневертебральные [3, 10]), в других – круг анализируемых потенциальных факторов риска был слишком мал и многие важные характеристики РА или терапии ГКС не рассматривались [11]. Таким образом, вопросы, у каких больных РА имеется максимальный риск переломов, кому из них в первую очередь назначать профилактические или лечебные мероприятия и на каком этапе, остаются нерешенными.
Цель исследования – охарактеризовать группы больных РА с переломами и без переломов в анамнезе для дальнейшего выделения возможных факторов риска переломов.
Материалы и методы исследования
Данная работа представляет собой фрагмент многоцентровой программы «Остеопороз при ревматоидном артрите: диагностика, факторы риска, переломы, лечение», проведенной в 2010-2011 г. и включавшей мужчин и женщин в возрасте 18 лет и старше с достоверным диагнозом «ревматоидный артрит» в соответствии с критериями Американской коллегии ревматологии (American College of Rheumatology, ACR) 1987 г., с исходной денситометрической оценкой МПК и возможностью динамического наблюдения на протяжении не менее 3 лет. Для настоящего исследования были отобраны 254 женщины в возрасте от 18 до 85 лет с давностью заболевания от полугода до 42 лет. На всех больных были заполнены специально разработанные тематические карты, данные внесены в таблицу Exсel для дальнейшей статистической обработки. Сведения о больных включали результаты опроса, оценку коморбидных состояний, осмотр, анализы крови (скорость оседания эритроцитов (СОЭ), тест на C-реактивный белок (СРБ), гемоглобин, общепринятые биохимические показатели), оценку активности заболевания (DAS28 – disease activity score) и опросник для оценки состояния здоровья (HAQ – Health Assessment Questionnaire). Пациенткам была выполнена рентгенография кистей и стоп, грудного и поясничного отделов позвоночника в боковой проекции. Подсчет общего числа эрозий и сужений суставных щелей по методу Sharp проведен у 108 больных, оценка индекса деформаций по методу Genant – у 173 больных в возрасте от 18 до 65 лет. МПК в поясничном отделе позвоночника (L1-L4) определена у 198 больных, в проксимальном отделе бедренной кости – у 184, в костях предплечья (средняя треть лучевой кости) – у 134 с использованием двухэнергетической рентгеновской абсорбциометрии (dual-energy X-ray absorbtiometry – DXA) на аппарате Hologic QDR1000. У женщин в постменопаузальном периоде диагноз остеопороза был установлен по T-критерию ≤ -2,5 стандартных отклонения (СО) от пика костной массы, у женщин с сохраненным менструальным циклом – по Z-критерию ≤ -2,5 СО в соответствии с рекомендациями Международного общества по клинической денситометрии 2007 г. [12]. Значения МПК от -1 до -2,5 СО по T- или Z-критерию у женщин после/до менопаузы соответственно свидетельствовали об остеопении.
Были проанализированы данные анамнеза: характер перелома (низкоэнергетический или полученный в результате травмы при падении с высоты собственного роста), возраст больных на момент возникновения перелома, возникновение перелома до/после наступления РА, менопаузы, количество и локализация переломов. Сведения о переломах подтверждены медицинской документацией или рентгенограммами.
Статистическая обработка материала выполнена с использованием программ Microsoft Excel, Bioistics Version 4.03, istic 6.
Результаты
254 больных РА были разделены на две группы. В 1-ю группу вошла 101 (39,8%) пациентка с низкоэнергетическими переломами в анамнезе, во 2-ю группу – 153 (60,2%) пациентки без переломов. Основные характеристики больных каждой группы представлены в табл. 1.
Средний возраст пациенток 1-й группы составил 59,8 ± 11,8 года, 2-й группы – 56,1 ± 11,4 года (р
Больше половины больных обеих групп имели III или IV рентгенологическую стадию РА по Штейнброкеру. При этом IV стадия РА встречалась достоверно чаще в группе больных с переломами (р 0,05).
Различий в оценке степени активности заболевания по показателю DAS28 между группами не выявлено. В обеих группах на момент исследования преобладали больные с умеренной степенью активности. Среднее значение показателя HAQ оказалось выше в группе больных с переломами – 1,720 ± 0,755 vs 1,431 ± 0,806 (р 2 баллов имели 39,5 и 24,8% женщин 1-й и 2-й группы соответственно (р
Внесуставные проявления РА отмечались у 58 (59,8%) пациенток с переломами и у 58 (39,5%) пациенток без переломов (р
Больных, получавших терапию ГКС свыше 3 месяцев, было достоверно больше в 1-й группе (78,2 vs 66,7%, р
Что касается терапии базисными противовоспалительными препаратами (БПВП), на момент обследования в 1-й группе меньшее количество больных получали БПВП (80,2 vs 89,5%, р
Особое внимание уделялось анализу показателей МПК (табл. 2). Так, остеопороз в поясничном отделе позвоночника (L1-L4), по данным рентгеновской денситометрии, был установлен у 42,7% больных 1-й группы и у 26,5% больных 2-й группы (р 0,05) соответственно. Остеопороз в ШБ также достоверно чаще наблюдали у больных с переломами в анамнезе по сравнению с пациентами без переломов (39,4 vs 24,1%, р 0,05) соответственно. В костях предплечья остеопороз диагностирован у 67,3% женщин в группе с переломами и у 41% – в группе без переломов (р
Мы сопоставили в группах частоту осложнений РА (амилоидоз и остеонекроз) и сопутствующих заболеваний (гипотиреоз, артериальная гипертония, сахарный диабет, эрозивно-язвенные поражения желудочно-кишечного тракта, хронические обструктивные заболевания легких), негативное влияние которых на состояние костной ткани подтверждено данными литературы. Сопутствующие заболевания были выявлены у 85 (84,2%) больных 1-й группы и у 108 (70,6%) пациенток 2-й группы (р
При анализе возраста больных на момент возникновения первого низкоэнергетического перелома, его характера и локализации, связи с РА, приемом ГКС и менопаузой выяснилось, что у 45 (44,5%) женщин перелом возник до начала РА в возрасте 26,5 ± 16 лет, у 56 (55,5%) – после начала заболевания. Средний возраст на момент перелома составлял 51,6 ± 13,7 года (рисунок). У 46 (46,5%) больных переломы возникли после наступления менопаузы, у 53 (53,5%) – до наступления. У 50 пациенток из 101 в анамнезе было более одного случая низкоэнергетического перелома. Всего установлено 178 случаев переломов. Наиболее частыми локализациями переломов оказались кости предплечья – 32 (18%) случая – и кости голени – 24 (13,5%) случая. Переломы позвонков (в том числе деформации с индексом по Genant
Мы выделили подгруппу больных (n = 20) с переломами, дебют заболевания у которых приходился на возраст от 16 до 30 лет (в период моделирования костной ткани и формирования пика костной массы). Средний возраст на момент возникновения первого перелома у этих пациенток составил 32,3 ± 17 лет. У 9 (45%) больных в подгруппе было более одного перелома, всего отмечено 37 случаев переломов, или 20,8% всех проанализированных переломов. На переломы предплечья пришлось 7 (21,9%) случаев в группе с дебютом РА от 16 до 30 лет, переломы голени – 4 (16,7%), переломы позвонков – 5 (26,3%), переломы бедра – 4 (40%) случая.
Обсуждение
Из 254 больных РА, включенных в исследование, более трети (39,8%) имели в анамнезе низкоэнергетические переломы. Согласно результатам анализа, полученным в ходе данного исследования, переломы ассоциировались с возрастом (59,8 ± 11,8 года), наступлением менопаузы, большей длительностью РА, в том числе свыше 10 лет. Также для больных с низкоэнергетическими переломами были характерны более частая терапия ГКС свыше 3 месяцев, длительный прием ГКС (в среднем 84,4 ± 67 месяцев) и кумулятивная доза в среднем 19,037 ± 18,724 г. У таких больных чаще отмечались внесуставные проявления, осложнения РА (амилоидоз и остеонекроз). Не вызвала сомнений связь между возникновением переломов и низкой МПК.
В отличном по дизайну исследовании S.Y. Kim, в котором ФР переломов определялись путем сопоставления больных РА и пациентов без РА, авторы установили, что высокому риску остеопоротических переломов подвержены лица в возрасте 65-74 лет (относительный риск (ОР) 2,18 для больных РА по сравнению с пациентками без РА). Однако наибольшее значение, по результатам данного исследования, имели предшествующие переломы (ОР 5,97, 95% доверительный интервал (ДИ) 5,29-6,75) и женский пол (ОР 1,89, 95% ДИ 1,73-2,07). Прием пероральных ГКС в анамнезе также имел значение (ОР 1,15, 95% ДИ 1,03-1,27). Авторами не отмечено существенного влияния снижения МПК на риск возникновения переломов у больных РА [13].
В самой масштабной по количеству участников работе британских ученых проанализированы наиболее значимые факторы риска переломов у больных РА и пациентов группы контроля. Показано, что больные РА имели повышенный риск переломов, особенно переломов бедра и позвонков. Наибольшее влияние на вероятность возникновения переломов (в частности, переломов бедра) оказали, по мнению авторов, длительность РА свыше 10 лет, низкий ИМТ, а также прием ГКС. Исследователи отметили, что риск переломов у больных РА оставался высоким даже при исключении при расчетах лиц, когда-либо принимавших ГКС: ОР составил 1,3 (95% ДИ 1,2-1,4) для остеопоротических переломов и 1,7 (95% ДИ 1,5-2) для переломов бедра. Как отметили сами авторы, незначительная роль ГКС в возникновении переломов, вероятно, связана с тем, что в данном исследовании лишь четверть больных РА принимали ГКС, что отражает ситуацию в Европе, но не в странах Нового Света (в том числе в США), где терапией ГКС охвачены до 75% больных РА [5].
В проспективном когортном исследовании японских ученых с участием 1733 женщин, больных РА, были определены наиболее значимые ФР переломов, в частности возраст старше 70 лет, высокие значения HAQ, низкий СРБ и переломы в анамнезе. О влиянии ограничения функциональных возможностей и снижения физической активности, которые в значительной мере отражаются при подсчете показателя HAQ, сообщалось неоднократно. В данном исследовании особенно высоко оценено значение данного показателя для риска возникновения переломов костей любой из анализируемых авторами локализаций [11]. В нашем исследовании группе больных РА с переломами в анамнезе также соответствовало высокое среднее значение HAQ.
При анализе показателей мы не получили статистически значимых различий и связи переломов с активностью РА по DAS28 и рентгенологической характеристикой заболевания по индексу Sharp на момент исследования. Субъективные оценки врача степени активности РА и функциональной недостаточности также не различались. В большинстве работ, посвященных изучению ФР переломов у больных РА, в которых выявлена связь между высокой активностью болезни и случаями переломов, помимо клинических параметров активности учитывали лабораторные показатели (СРБ, СОЭ, ревматоидный фактор и др.) [1, 6]. Другой причиной таких результатов может быть особенность выборки больных для исследования (например, только госпитализированные в лечебно-профилактические учреждения больные, текущая активность заболевания большинства из которых была высокой). В нашем исследовании были использованы данные как амбулаторных, так и стационарных больных. Более чем у половины из них активность заболевания была умеренной. Следует отметить, что для оценки вклада воспалительной активности в риск возникновения переломов необходимо наблюдать больных в динамике с анализом эффективности антиревматической терапии и приверженности лечению.
Нельзя не сказать и о связи между низкими показателями МПК во всех анализируемых областях и переломами у наших больных. Как известно, характеристика костной ткани (масса, плотность, архитектоника, степень минерализации и др.) – показатель прочности кости, а остеопороз – чрезвычайно значимый ФР возникновения переломов у больных РА. Негативная роль снижения МПК неоднократно подтверждена в зарубежных исследованиях ФР переломов [1, 10, 14, 15]. Казалось бы, связь между остеопорозом и риском возникновения переломов не должна вызывать сомнений: лица с низкой костной массой подвержены большему риску переломов [16]. Тем не менее, по литературным данным, этот вопрос остается спорным [4, 8, 17] и требует дальнейшего изучения. РА является фактором, способствующим потере МПК, заболеванием, увеличивающим риск развития остеопороза (уровень доказательности А) [18].
Таким образом, нами получены и проанализированы сведения о больных РА с переломами и без таковых в анамнезе, включающие антропометрические, клинико-рентгенологические характеристики и результаты денситометрии. Представлены данные о случаях низкоэнергетических переломов в анамнезе у больных РА и предварительные результаты сравнительного анализа ФР в группах больных с переломами и без таковых. Более детальный (корреляционный и дискриминантный) последующий анализ позволит установить вклад каждого фактора и определить индивидуальный прогноз развития переломов у больных РА, разработать тактику лечебно-профилактических мероприятий.
Источник
Ревматоидный артрит (РА) одна из самых таинственных и древних болезней. Следы ревматоидного артрита обнаружены на остатках скелетов индейцев в Теннесси, США, датируемых 4500 годом до нашей эры.
РА принадлежит к классу аутоиммунных заболеваний – когда организм, вместо того, чтобы уничтожать естественных врагов (болезнетворные микробы, опухолевые клетки и т.д.), вдруг ополчается против собственных здоровых тканей и принимается их разрушать. При ревматоидном артрите страдают соединительные ткани суставов. Также могут воспаляться околосуставные ткани – связки и мышцы.
Вирус-невидимка
Несмотря на все успехи современной науки, причины ревматоидного артрита до сих пор не установлены. Некоторые исследователи считают, что развитие этого заболевания провоцируется неким вирусом, который исчезает к моменту появления заболевания. p>
Болезнь играет в прятки
Как и большинство аутоиммунных заболеваний, ревматоидный артрит идет «волнами», чередуя периоды обострения и ремиссии. Даже при тяжелых формах боль может уменьшиться или вовсе исчезнуть на длительный срок, даже на несколько лет. Иногда больным начинает казаться, что они совершенно исцелились. Увы. К сожалению, это не так. Ревматодидный артрит – хроническое заболевание, и в настоящее время излечить его полностью невозможно. Если кто-нибудь обещает средство, которое избавит вас от ревматоидного артрита, можете быть уверены, что перед вами обманщик.
Факторы риска
В России ревматоидным артритом, по различным данным, болеет от 1 до 2% населения. Чаще болеют люди после 30 лет. При этом женщин среди больных в 5 раз больше, чем мужчин.
- Наследственная предрасположенность.
- Инфекция (примерно в 50% случаев ревматоидному артриту предшествовало ОРЗ, грипп, ангина, другие инфекционные заболевания).
- Реактивный или инфекционный артрит.
- Сильное переохлаждение.
- Эмоциональный стресс (развод, смерть близких, экзменационная сессия)
- Некоторые черты характера: высокая степень ответственности, тревожность, склонность к депрессиям (такие люди предрасположены к психологическим травмам, что ведет к снижению иммунитета).
Симптомы
- Пястно-фаланговые суставы («костяшки») указательного и среднего пальцев рук воспаляются, припухают, становятся болезненными.
- Воспаляются и припухают лучезапястные суставы.
- Одновременно с воспалением суставов рук, как правило, поражаются и мелкие суставы стоп.
- Боль у основания пальцев ног.
- Воспаление симметричное (в подавляющем большинстве случаев поражаются те же суставы на обеих руках, те же суставы на обеих ногах).
- Боли усиливаются ближе к утру и до полудня очень интенсивны.
- Боль спадает после полудня и возобновляется около 3-4 часов ночи.
- Утренняя скованность, ощущение затекшего тела.
- Чувство слабости.
- Ухудшение сна и аппетита.
- Повышение температуры до 37,2-38°С.
- Лихорадка.
- Потеря веса.
Если у вас появились хотя бы некоторые из этих симптомов, немедленно обратитесь к врачу. Чем раньше начать лечение ревматоидного артрита, тем больше шансов сохранить функции суставов и продолжить активную жизнь.
Диагноз
Существует несколько способов диагностировать ревматоидный артрит:
- Анализ на ревматоидный фактор (РФ, Rheumatoid factor, RF). Ревматоидным фактором называются особые белки, аутоантитела к иммуноглобулинам класса G (IgG). Эти белки нападают на «родные» для организма иммуноглобулины класса G, потому что те видоизменились под влиянием вируса или других воздействий. При ревматоидном артрите показатель РФ повышен. Однако при ювенильном ревматоидном артрите (встречается у детей и подростков) РФ часто бывает отрицательным, а у пожилых людей повышение РФ может определяться без клинических проявлений ревматоидного артрита. Поэтому один этот анализ не позволяет однозначно поставить диагноз. Он должен быть подтвержден другими клиническими и лабораторными исследованиями.
- Рентгенологическое исследование на ранней стадии заболевания может не показывать изменений. В дальнейшем на снимках становятся видны типичные для ревматоидного артрита изменения суставов.
- Артроцентез – пункция суставов. С помощью шприца берется проба суставной жидкости, которую затем исследуют. Артроцентез используют также в лечебных целях – чтобы удалить избыток жидкости при воспалении или ввести в сустав лекарственные препараты.
Протекание и результат
Ревматоидный артрит – не та болезнь, на которую можно не обращать внимания. По мере развития болезни к поражению суставов добавляются различные нарушения в работе внутренних органов. Может произойти ревматоидное поражение легких, сердца, печени, почек, кишечника, сосудов. Поэтому так важно начать терапию уже на ранней стадии заболевания.
Лекарственные препараты и лечение
Первую помощь оказывают противовоспалительные или быстродействующие препараты: нестероидные противовоспалительные препараты (НПВП) и гормоны (кортикостероиды).
1) НПВП: ацетилсалициловая кислота (аспирин), флексен, диклофенак, индометацин, пироксикам, бруфен и др. Они снимают боль и облегчают жизнь больного. Подбираются врачом индивидуально для каждого больного методом «проб и ошибок», поскольку для разных больных эффективны различные препараты.
- Действуют только в период их применения. К сожалению, длительный прием вызывает побочные эффекты. Чаще всего плохо влияют на желудок. Поэтому больным, у которых был гастрит или язва, НПВП назначают с осторожностью.
- Чтобы защитить слизистую оболочку желудка, врач может назначить гастропротекторы: мизопростол и препараты группы ранитидина. Если вы принимаете НПВП, помните, что их следует принимать после еды.
- В настоящее время разработана новая группа НПВП – селективные противовоспалительные средства (например, «Мовалис»). Они могут применяться более длительно. Риск развития побочных эффектов у них существенно снижен.
2) Кортикостеродные гормоны (преднизолон, метилпред, гидрокортизон и т. д.) уменьшают боль, утреннюю скованность, слабость и лихорадку. Их назначают в виде таблеток или инъекций, иногда вводят непосредственно в сустав.
- При длительном применении также имеют сильные побочные эффекты: повышение массы тела, ухудшение иммунитета, гипертония, разрушение костей.
- Короткие (до 10 дней) курсы стероидов практически не вызывают побочных эффектов.
- Важно помнить, что при длительном приеме (2 недели и больше) их отмену можно производить только постепенно и только под наблюдением врача.
Наружно для уменьшения боли и воспаления может применяться димексид. Его наносят на суставы в виде аппликаций. Улучшение отмечается после 6-7 дней и становится более выраженным после двух недель применения.
Болезнь-модифицирующие или базисные препараты – воздействуют на основу, «базис» болезни. Вызывают ремиссию и предотвращают разрушение суставов. Они не являются противовоспалительными и болеутоляющими. Не дают быстрого эффекта, рассчитаны на длительное применение. Результаты обычно начинают появляться через месяц после начала приема.
Чаще всего используют препараты пяти групп:
- Соли золота (кризанол, ауранофин) приносят существенное облегчение примерно 70% больных. Однако в последнее время их стали применять реже из-за побочных эффектов: кожная сыпь, воспаление слизистой рта, угнетение кроветворения, повреждение почек.
- Антималярийные средства (делагил и плаквенил). В прошлом ими лечили малярию (тропическую лихорадку). Но в 20-м веке ревматологи заметили, что при очень длительном применении делагил и плаквенил замедляют ревматоидный процесс. Увы, и здесь не обходится без побочных эффектов. Возможно расстройство желудка, кожная сыпь, мышечная слабость и нарушение зрения. Если вы принимаете Плаквенил, вам необходимо регулярно проходить обследование у офтальмолога.
- Д-пеницилламин (купренил) назначают, когда золототерапия не помогает или вызывает побочные эффекты. Но Д-пеницилламин тоже весьма токсичен. Осложнения могут проявляться кожной сыпью, расстройствами желудка и кишечника, воспалением почек, желтухой, возникающей из-за застоя желчи, а также изменением состава крови. Поэтому в случае применения Д-пеницилламина больной в первое время регулярно сдает анализы крови и мочи. Осложнения проявляются в первые два месяца применения лекарства, но при отмене препараты исчезают. Д-пеницилламин противопоказан беременным и пациентам с заболеваниями заболевания крови и почек.
- Сульфасалазин (антимикробный препарат) переносится лучше, чем препараты золота и Д-пеницилламин. Побочные эффекты (расстройство желудка и кожная сыпь) развиваются только у 10-20% больных. Это «долгоиграющий» препарат, улучшение состояния наблюдается обычно после трех месяцев его применения.
- Иммуносупрессоры. Это – «подарок» онкологов, которые применяют эти лекарства (метотрексант, азатиоприн, циклофосфан, хлорбутин, лейкеран) для подавления иммунной системы и торможения деления клеток, раковых в том числе. В ревматологии их используют в значительно меньших (в 3-10 раз) дозах, чем в онкологии, что уменьшает риск побочных эффектов. Однако у 15-20% больных все же наблюдается расстройство желудка и нарушения мочеиспускания. После отмены препарата осложнения проходят. Улучшения самочувствия можно ожидать в течение месяца после назначения препарата.
Ревматоидный артрит – не только загадочная, но и капризная болезнь, требующая «подхода». Разным больным помогают разные лекарства; на то, чтобы правильно подобрать их, иногда уходит довольно длительное время. Бывает, что через несколько месяцев после приема приходится менять препарат и снова ждать результатов. Если вы проходите лечение, проявляйте терпение. Не прекращайте прием лекарств, не посоветовавшись с врачом.
Помимо медикаментозного лечения используется:
- Лазерная терапия. Оказывает мягкий противовоспалительный эффект. Применяется как отдельный метод лечения и в сочетании с базисной терапией. Облучают не суставы, как можно было бы ждать, а локтевую вену. Излучение воздействует на кровь, циркулирующую внутри организма. В результате нормализуется иммунитет, улучшается кровоснабжение органов и тканей, уменьшается любое воспаление и подавляются очаги инфекции. Назначают 15-20 процедур через день. Лучшие результаты дает при мягкой форме заболевания. При тяжелых формах малоэффективна.
- Криотерапия (лечение местным замораживанием) – дорогостоящий, но эффективный метод лечения. Улучшение наблюдается у 60-70% пациентов. Не имеет противопоказаний. Применяется как в острой, так и в хронической фазе ревматоидного артрита.
- Массаж. Проводится в период ремиссии.
- Лечебная физкультура. Укрепляет мышцы, поддерживает подвижность суставов. Лучший вид физической нагрузки – плавание, потому что оно устраняет гравитационную нагрузку на суставы.
- Хирургическое лечение. Применяется для устранения деформаций и восстановления функции суставов. Широко применяется малоинвазивная хирургия (артроскопия). В некоторых случаях проводят полную замену разрушенного сустава протезом.
Как предотвратить ревматоидный артрит?
Если у вас в семье есть больные ревматоидным артрозом, риск заболеть им существенно повышается. Это вовсе не обязательно должно произойти, но все-таки в этом случае лучше проходить регулярные обследования.
Ревматоидный артрит может развиться и у совершенно здорового человека и перейти в острую форму в течение нескольких суток.
Средство для полного излечения пока не найдено, хотя исследования в этом направлении продолжаются. Однако своевременно начало лечения способно существенно улучшить состояние пациента, сохранить суставы и продлить активную жизнь.
Вот еще несколько советов:
- Помните, что есть связь между иммунной и психологической системой. Если вы склонны к тревожности, депрессии и/или у вас в жизни стрессовая ситуация, обратитесь за помощью к психологу.
- Поддерживайте нормальный вес.
- Регулярно выполняйте физические упражнения.
- Избегайте переохлаждения.
- Не переносите грипп и ангину на ногах, своевременно лечите инфекционные заболевания.
Источник
