Заболевания позвоночника в практике терапевта

В статье проведено обобщение современных подходов к диагностике и лечению синдрома боли в спине на уровне амбулаторной терапевтической службы. Приведены алгоритмы стандартных и минимально необходимых диагностических манипуляций, очерчены показания для назначения консультаций смежных специалистов.
Введение
Синдром боли в спине остается одной из самых частых причин обращения к врачу как в нашей стране, так и за рубежом [1, 2]. Согласно последним эпидемиологическим исследованиям, в течение жизни боль в спине возникает у 70–90% населения, преимущественно у людей трудоспособного возраста, а у 20–25% регистрируется ежегодно [3]. Глобальное исследование заболеваемости населения (Global Burden of Disease Study) признало боль в спине главной причиной нетрудоспособности в мире [4]. Боль в нижней части спины (БНС) является одной из самых частых причин обращения к врачам самых разных специальностей. Европейское многоцентровое исследование продемонстрировало, что хронической болью страдает более 20% жителей Европы, при этом большинство пациентов испытывало боль именно в нижней части спины [5].
При этом на терапевтическое звено оказания медицинской помощи падает наибольшая нагрузка по работе с данной категорией пациентов. Согласно опросу, проведенному Всероссийским центром изучения общественного мнения (ВЦИОМ) в ноябре 2017 г., охватившему более 700 жителей РФ трудоспособного возраста (от 22 до 45 лет), испытывавших боли в спине в настоящее время или в течение последнего года, выявлено, что более 1/3 из них обращались именно к терапевту с жалобами на боли в спине (рис. 1).
Диагностический поиск при БНС
Очевидно, что боль как патологический феномен является целой цепью изменений на разных уровнях организма [2]. Поначалу защитный механизм, сигнализирующий о проблеме, позднее становится серьезным и, подчас, самостоятельным страданием. Как писал еще Авиценна: «Боль помогает врачу распознать заболевание, нередко указывая правильный путь лечения. Такая боль приносит пользу, подобно огню, когда он согревает, а не сжигает; подобно воде, когда она орошает, а не затопляет, подобно ветру, когда он освежает, а не разрушает».
Поэтому задачи терапевтической службы — не столько постановка точного топического диагноза, сколько скрининг и анализ основных жалоб и симптомов, исключение серьезной патологии (так называемых «красных флагов»), назначение противоболевой терапии, которая сама по себе может дать подсказки о причине развития болевого синдрома, и при необходимости направление пациента к узкому специалисту для уточнения диагноза [1, 3].
БНС характеризуют как боль, мышечное напряжение и/или скованность, локализующиеся между нижней парой ребер и ягодичными складками с иррадиацией в нижние конечности или без таковой. Доброкачественная скелетно-мышечная боль в спине не считается нозологической единицей. Высокая распространенность и частое отсутствие конкретной объективно визуализируемой анатомической причины заставили выделить синдром БНС в МКБ-10 в качестве регистрационной, а не нозологической категории М 54.5. Для этой формы БНС не выявлено связи между тяжестью морфологических изменений позвоночника (по данным компьютерной и магнитно-резонансной томографии) и выраженностью боли в спине. Так, явная патология межпозвонковых дисков зачастую обнаруживается у практически здоровых людей, при этом выявление патологических изменений в межпозвонковых дисках не приводит к развитию боли в спине в дальнейшем [2, 3, 5].
С практической точки зрения удобно выделять 3 основные причины болей в спине.
Неспецифическая боль в спине (частота встречаемости — 85–90%). Этот термин означает, что не удалось выявить серьезную патологию (заболевание), явившуюся причиной боли: инфекцию, травму, воспаление, опухоль, остеопороз, ревматоидный артрит, анкилозирующий спондилит, заболевание соединительной ткани и др. Помимо этого, должны отсутствовать специфические признаки вовлечения в процесс корешков спинномозговых нервов (радикулопатия — 1–5%, синдром конского хвоста — до 2%) и стеноза спинномозгового канала.
Специфические причины (частота встречаемости 4–7%):
перелом позвоночника;
первичные и метастатические опухоли позвоночника;
миеломная болезнь;
спондилоартрит;
остеомиелит;
эпидурит;
сирингомиелия;
опухоли спинного мозга и спинномозговых корешков;
заболевания внутренних органов.
Боль, вызванная компрессионной радикулопатией, стенозом поясничного канала (частота встречаемости — 7%).
С учетом того, что большинство заболеваний внутренних органов находятся в сфере ответственности терапевта, становится ясно, что именно этому врачу чаще всего приходится решать проблему болей в спине.
В помощь терапевтам разработаны относительно простые диагностические алгоритмы и опросники [3, 6]. Не требующий специальных инструментов, простой, но скрупулезный диагностический поиск позволяет уже на амбулаторном терапевтическом приеме не только верифицировать самые распространенные причины болевого синдрома, но и заподозрить серьезные заболевания, требующие неотложных мер, диагностических процедур, направления к узким специалистам (табл. 1).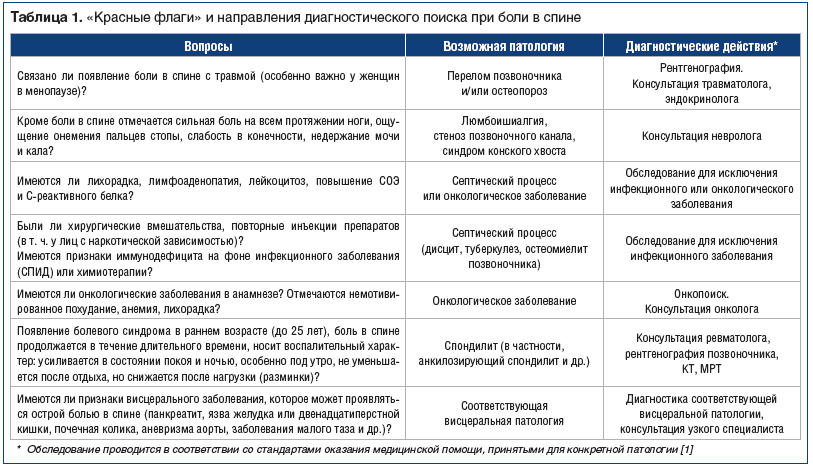
Минимальный лабораторный диагностический набор состоит из анализа крови и мочи, оценки скорости клубочковой фильтрации, концентраций глюкозы и — при возможности — высокоточной оценки С-реактивного белка.
Минимальный инструментально-диагностический набор состоит из измерения артериального давления, ЭКГ, рент-
геновского исследования органов грудной клетки и УЗИ
органов брюшной полости и забрюшинного пространства.
Алгоритм действий врача-терапевта представлен на рисунке 2.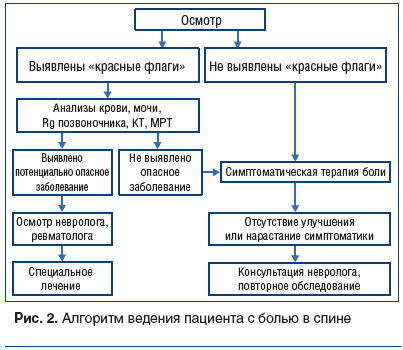
Терапия боли в спине
Сложности в достижении адекватного обезболивания в рутинной практике определяются упомянутой выше коморбидностью, неизбежной полипрагмазией и необходимостью долгосрочной терапии болевого синдрома [7, 8]. У коморбидных пациентов с целой палитрой соматических заболеваний предпочтительным критерием выбора становится безопасность лекарственного препарата и безопасность лекарственного взаимодействия.
Проведенные эпидемиологические исследования показывают, что не более чем у 20% пациентов удается обеспечить адекватное обезболивание. Это связано с использованием недостаточно эффективных либо устаревших лекарств, необоснованных схем применения, рефрактерностью у пациентов, часто использующих анальгетики, нежелательными побочными реакциями и др. [8].
У большинства пациентов проводимая терапия эффективно купирует боли в течение 4 нед. Однако почти у 73% больных в течение первого года наблюдения развивается как минимум одно обострение [7]. Также отмечено, что 20–25% больных продолжают испытывать боль в спине, т. е. страдание становится хроническим, что приводит к существенному возрастанию нагрузки и на органы здравоохранения, и на бюджет в целом: на эту когорту больных тратится до 80% средств здравоохранения [7].
Самым частым средством купирования как острых, так и хронических болевых синдромов в отечественной и мировой практике являются нестероидные противовоспалительные препараты (НПВП). Это корреспондирует и с Рекомендациями по ведению хронической боли [9]. Ключевыми препаратами они остаются и при лечении болей в спине [10]. Выбор НПВП должен быть обдуманным и взвешенным, с оценкой соотношения риска и пользы конкретного препарата.
Чем в основном определяется сегодня безопасность терапии НПВП? Ответ, очевидно, лежит в области коморбидности пациентов, отмечаемой в последнее время не только у пожилых, но и у относительно молодых больных. Так, риск повреждения слизистой оболочки органов желудочно-кишечного тракта (в т. ч. НПВП-гастропатии) есть у большинства пациентов отделений кардиологии, терапии, гастроэнтерологии. Причем кровотечения, связанные с собственно язвенной болезнью, составляют лишь небольшую часть всех желудочно-кишечных кровотечений (ЖКК) в структуре смертельных осложнений, явившихся причиной летального исхода [11]. При безальтернативности применения НПВП при болевых синдромах одной из основных задач менеджмента боли остается выбор правильного препарата и его лекарственной формы [10, 11].
Понимание различной роли изоформ циклооксигеназы (ЦОГ) в механизмах воспаления и генезе побочных эффектов препаратов НПВП привело к разработке и внедрению в широкую клиническую практику наряду с «классическими» и относительно селективных и высокоселективных ЦОГ-2 ингибиторов. Эти препараты имеют лучший профиль гастроэнтерологической безопасности. Однако практика их применения сопровождается сообщениями о кардиоваскулярных рисках высокоселективных ЦОГ-2 ингибиторов. Результаты клинического исследования VIGOR, в котором проводилось сопоставление эффективности и безопасности напроксена и рофекоксиба в симптоматической терапии ревматоидного артрита, показали, что при более низкой частоте желудочно-кишечных побочных эффектов у пациентов, получавших рофекоксиб, частота инфаркта миокарда в этой группе составила 0,4% в сравнении с 0,1% у пациентов группы напроксена [12]. Существенное увеличение риска кардиоваскулярных катастроф при использовании рофекоксиба было получено и в исследовании APPROVe [13]. Поэтому интерес исследователей и клиницистов при применении НПВП при острой и хронической боли смещается к препаратам со сбалансированной активностью в отношении ЦОГ [14]. Особенно это важно для коморбидных пациентов, т. к. сердечно-
сосудистые заболевания и поражения ЖКТ относятся к самым частым вариантам коморбидности.
Представителем НПВП, обладающим благоприятным профилем ингибирования активности ЦОГ, является ибупрофен, считающийся и одним из наиболее изученных анальгетиков в группе НПВП. При лечении сильных болевых синдромов, требующих быстрого купирования, перспективной оказалась комбинация ибупрофена с парацетамолом, обеспечивающая потенцирование действия обоих компонентов, возможность снижения дозировок с минимизацией риска побочных эффектов [15]. Оценка рисков развития желудочно-кишечных осложнений при терапии различными НПВП проведена в исследованиях J. Castellsague et al., А.Е. Каратеева и др., результаты приведены на рисунке 3 [16, 17].
Риски сердечно-сосудистых осложнений при терапии различными НПВП оценены в исследовании С. Varas-Lorenzo et al. (2013), результаты приведены на рисунке 4 [18].
Собственная анальгетическая эффективность предлагаемой комбинации (ибупрофен 200 мг + парацетамол 500 мг, например, препарат Нурофен Лонг) превосходит эффективность монокомпонентных НПВП и даже комбинированных препаратов, содержащих кодеин (рис. 5, 6) [19]. Эта комбинация и в одинарной, и в двойной дозе (ибупрофен 400 мг + парацетамол 1000 мг) имеет самый низкий коэффициент NNT, превосходя по эффективности диклофенак и декскетопрофен [20].
![Рис. 6. Сравнительная эффективность комбинированных анальгетиков [19] Рис. 6. Сравнительная эффективность комбинированных анальгетиков [19]](https://www.rmj.ru/upload/medialibrary/9da/13-7.png)
Двойное слепое плацебо-контролируемое рандомизированное исследование S.E. Daniels et al. (n=600) показало, что комбинация ибупрофен 200 мг + парацетамол 500 мг, содержащаяся в препарате Нурофен Лонг, обеспечивает сопоставимое и даже более эффективное обезболивание, чем комбинированные кодеинсодержащие препараты [19].
Современная технология Synchro-Tech™ позволяет быстро высвобождать компоненты препарата, при этом эффективный обезболивающий эффект развивается уже к 15-й мин, достигает максимума к 40 мин и продолжается до 8 ч. Клинически важным оказывается и наличие противовоспалительного эффекта препарата Нурофен Лонг, реализуемого за счет нескольких механизмов: ингибирования ЦОГ, снижения выработки простагландинов на центральном уровне регуляции, уменьшения выработки провоспалительных медиаторов на локальном уровне, ингибирования миграции лейкоцитов в очаг воспаления.
Терапия болевого синдрома в спине может требовать дополнительного назначения и препаратов, содержащих витамины группы В, миорелаксантов, применения аппаратных методов лечения, физиотерапии, когнитивно-поведенческой терапии, которую ряд исследователей относит к первостепенным подходам. При всей обоснованности этих рекомендаций именно успешность (скорость и мощность) обезболивания определяет впечатление пациента от назначений врача, формирует уровень доверия и повышает комплаентность, что в конечном итоге служит залогом эффективности терапии.
Заключение
Лечением болевых синдромов в спине занимаются врачи разных специальностей, однако в первую очередь такие пациенты обращаются на амбулаторный прием к врачутерапевту. Этот синдром требует вдумчивой диагностики и терпеливого подхода к терапии с использованием современных лекарственных средств и немедикаментозных подходов.
Источник
ВВЕДЕНИЕ
Боль в спине объединяет широкий спектр нарушений состояния костных и мышечно-связочных структур позвоночника, занимает второе место по частоте обращений в поликлинику и третье – по количеству госпитализаций.
Глобальное исследование заболеваемости населения (Global Burden of Disease Study) признало боль в спине главной медицинской причиной снижения качества жизни в мире и России.
Боль в спине является междисциплинарной медицинской проблемой, но тем не менее первичное обращение этих пациентов осуществляется к терапевтам и врачам общей практики, на которых лежит ответственность за своевременную дифференциальную диагностику и назначение полного комплекса терапии в тех случаях, когда боль в спине не является проявлением серьезного или угрожающего жизни заболевания.
Консенсус экспертов призван систематизировать известные методы диагностики, лечения и вторичной профилактики боли в спине для их обязательного применения в поликлинике терапевтом или врачом общей практики.
ОПРЕДЕЛЕНИЕ
МКБ-10 определяет боль в спине (M54 «Дорсaлгия») как симптом, а не как нозологическую единицу, проводя разделение в зависимости от локализации.
С практической точки зрения удобно выделять три основные причины болей в спине:
1) неспецифическая (частота встречаемости 85–90%).
Термин «неспецифическая боль в спине» означает, что не удалось выявить серьезную патологию (заболевание), явившуюся причиной боли: инфекцию, травму, воспаление, опухоль, остеопороз, ревматоидный артрит и анкилозирующий спондилит, заболевание соединительной ткани и др. Помимо этого, должны отсутствовать специфические признаки вовлечения в процесс корешков спинномозговых нервов (радикулопатия и синдром «конского хвоста») и стеноза спинномозгового канала;
2) специфическая: опухоли, в том числе метастатические; спондилоартрит, воспаления, переломы позвонков и заболевания внутренних органов (частота встречаемости 4–7%);
3) боль, вызванная компрессионной радикулопатией, стенозом поясничного канала (частота встречаемости 7%).
ФАКТОРЫ РИСКА РАЗВИТИЯ НЕСПЕЦИФИЧЕСКОЙ БОЛИ В СПИНЕ
Среди них тяжелый физический труд, частые сгибания и наклоны туловища, подъем тяжестей, сидячий образ жизни, а также вибрационные воздействия. В группе риска находятся лица, чей труд связан с неадекватными для позвоночника нагрузками, а также люди, которые вынуждены длительно находиться в статическом напряжении, длительном сидячем положении: профессиональные водители, офисные работники.
У подавляющего большинства пациентов неспецифическая боль в спине проходит в течение нескольких дней или недель, однако в 2–10% случаев она принимает хроническое течение.
КЛИНИЧЕСКИЙ МОДУЛЬ
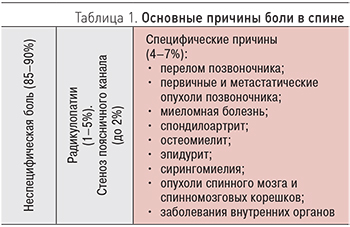 Основные причины боли в спине приведены в табл. 1.
Основные причины боли в спине приведены в табл. 1.
Классификация
В зависимости от длительности боли она подразделяется на:
- острую (продолжительность до 12 нед);
- хроническую (более 12 нед).
Клиническая картина
Учитывая, что чаще всего боль локализуется в нижней части спины, в последующем тексте Клинических рекомендаций большее внимание будет уделено боли именно в нижней части спины (БНЧС)3.
Как правило, боль в нижней части спины возникает остро после физической нагрузки, неловкого движения, переохлаждения, усиливается при движениях, в определенной позе и уменьшается после отдыха, растирания или разминания болезненных мышц. Боли могут ограничивать объем произвольных движений. О вовлечении в патологический процесс корешков можно говорить при выявлении чувствительных, рефлекторных или двигательных нарушений, простреливающих болей, иррадиирующих в нижние конечности.
ДИАГНОСТИЧЕСКИЙ МОДУЛЬ
При первичном обращении пациента с болью в нижней части спины в поликлинику необходимо исключить «красные флаги» (табл. 2) и при их наличии провести дополнительные обследования и/или направить на консультацию к специалистам. Распределение обязанностей среди специалистов приведено в табл. 3.
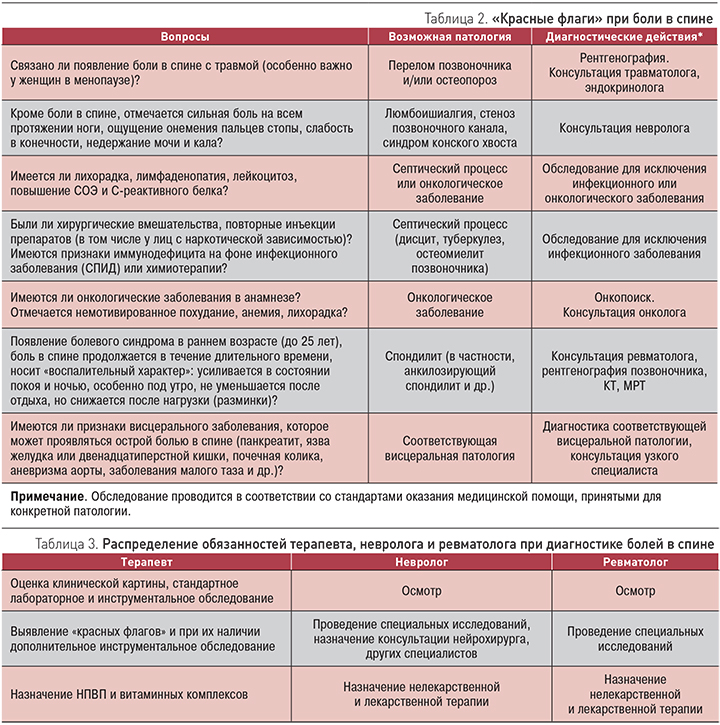
Основные вопросы, которые нужно задавать при опросе и осмотре пациента с болью в спине для исключения угрожающей жизни патологии, требующей дополнительного обследования и консультации узкого специалиста, приведены в табл. 4.
Стандартное терапевтическое обследование обязательно включает дифференциальную диагностику заболеваний и выявление лихорадки, похудания, изменения формы суставов, цвета кожных покровов, лимфаденопатии, гепатолиенального синдрома и др.
Для оценки выраженности и динамики болевого синдрома используется визуально-аналоговая шкала (ВАШ) (рис.).
Минимальный лабораторный диагностический набор состоит из анализа крови и мочи, оценки скорости клубочковой фильтрации, концентраций глюкозы и при наличии возможности высокоточного С-реактивного белка.
 Минимальный инструментальный набор состоит из измерения артериального давления, ЭКГ, рентгеновского исследования органов грудной клетки и УЗИ органов брюшной полости и забрюшинного пространства.
Минимальный инструментальный набор состоит из измерения артериального давления, ЭКГ, рентгеновского исследования органов грудной клетки и УЗИ органов брюшной полости и забрюшинного пространства.
Инструментальные методы (рентгенография позвоночника, КТ или МРТ, сцинтиграфия, денситометрия) назначаются терапевтом при наличии «красных флагов».
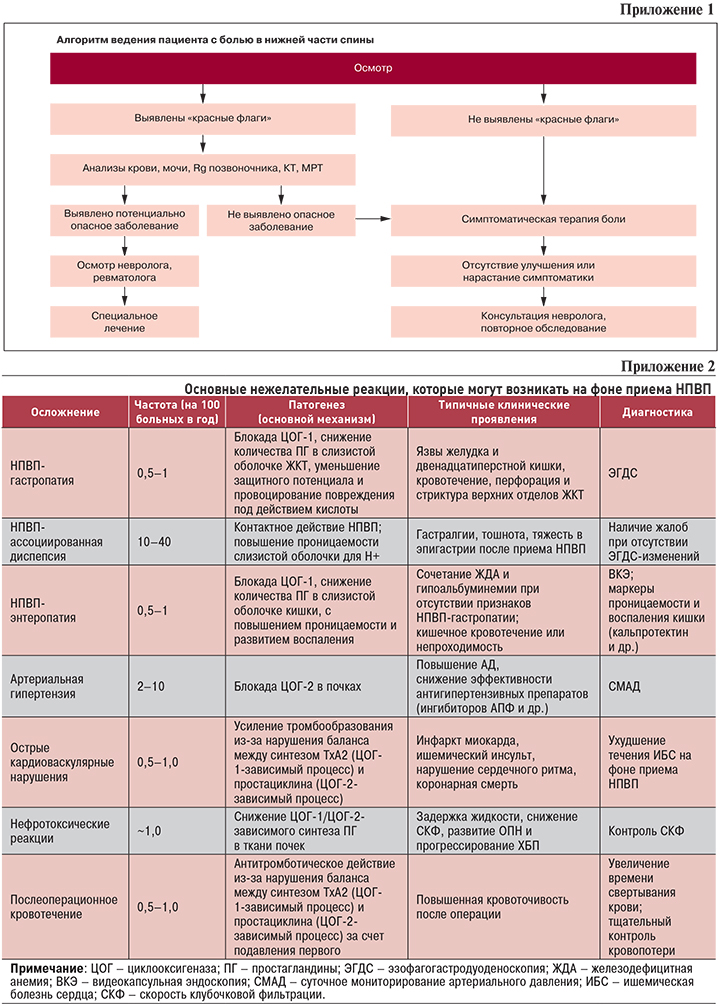
Алгоритм ведения пациента с болью в спине представлен в Приложении 1.
ТЕРАПЕВТИЧЕСКИЙ МОДУЛЬ
Лечение боли в спине
К общим принципам лечения болей в спине относится информирование пациента об основных причинах боли в спине, о роли активного образа жизни и дозированной физической нагрузки, избегании длительного постельного режима.
Общая терапия болевого синдрома в спине предусматривает применение средств, влияющих на патогенетические основные механизмы: воспаление, болезненный мышечный гипертонус, нарушение трофики нервной ткани и др.
Нестероидные противовоспалительные препараты (НПВП)
Основные положения по использованию НПВП при болях в спине:
- НПВП назначаются сразу же после установки диагноза, перорально в средней или максимальной терапевтической дозе.
- Инъекционные формы НПВП могут использоваться в течение первых 2–5 дней, согласно инструкции, при наличии выраженной боли или невозможности перорального приема.
- Длительность курса НПВП определяется временем, необходимым для максимально полного купирования боли и восстановления функции опорно-двигательного аппарата.
- Критерием хорошей эффективности является уменьшение боли не менее чем на 50% от исходного уровня и не позднее 5–7 дней после назначения препарата в полной терапевтической дозе.
- Неэффективность терапии (уменьшение интенсивности боли менее 20% от исходного уровня) с помощью адекватных доз НПВП в течение 2–4 нед служит основанием для назначения консультации невролога.
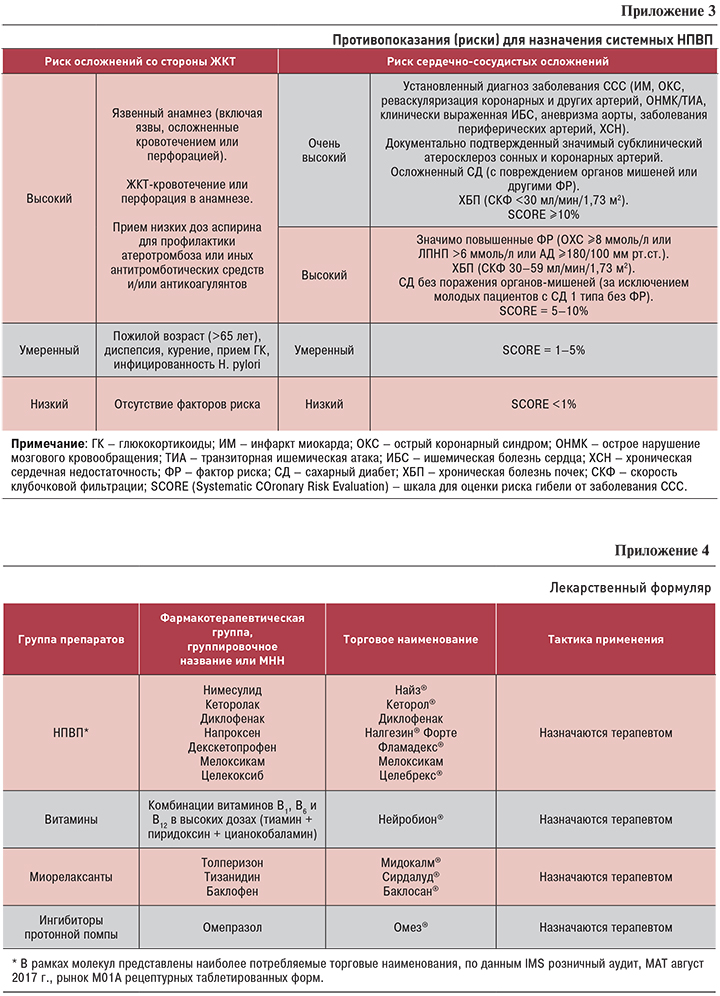
- При назначении НПВП всегда следует учитывать риск развития нежелательных явлений (см. Приложение 2). Не следует комбинировать два и более различных препарата этой группы, а также использовать дозы, превышающие рекомендованные.
- Во всех случаях для предупреждения нежелательных реакций НПВП должны назначаться ингибиторы протонной помпы (например, омепразол, рабепразол).
- Локальные формы НПВП (мази, гели и др.) следует использовать лишь при умеренной/слабой боли, а также при наличии противопоказаний для системных НПВП.
Тактика назначения широко применяемых НПВП
Кеторолак
Традиционный НПВП (неселективный ингибитор циклооксигеназы) с высоким анальгетическим потенциалом. Кеторолак целесообразно использовать при сильной боли в спине, вызывающей значительные страдания и нарушения функции («не могу из-за боли встать»). В начале лечения может применяться парентерально в виде в/м или в/в инъекций по 30 мг 3–4 раза в сутки, на срок до 2 сут. Затем переходят на пероральный прием по 10 мг 3 раза в день. Общая длительность приема не более 5 дней.
Напроксен
Традиционный НПВП (неселективный ингибитор ЦОГ-2), который используется для купирования умеренной или выраженной боли. Назначается в дозе 500 мг 2 раза в день после приема пищи. Для купирования БС обычно требуется курс 2–4 нед. Напроксен достаточно часто вызывает нежелательные реакции со стороны ЖКТ, но при этом считается наиболее безопасным НПВП в отношении сердечно-сосудистой системы. Препарат уменьшает натрийуретический и диуретический эффект фуросемида; может усилить гипотензию, вызываемую бета-адреноблокаторами.
Нимесулид
Умеренно селективный ингибитор ЦОГ-2 с благоприятным сочетанием высокой эффективности, хорошей переносимости и финансовой доступности, что позволяет рассматривать его как средство выбора для лечения скелетно-мышечной боли. Нимесулид назначается при умеренной или выраженной боли в спине перорально по 100 мг 2 раза в день 2–4 нед.
Целекоксиб
Высокоселективный ингибитор ЦОГ-2 с минимальным риском развития гастропатии. Применяется в дозе 200 мг 2 раза в сутки, с последующим переходом на 200 мг 1 раз, для поддерживающей терапии. При острой боли рекомендованная однократная стартовая доза составляет 400 мг с последующим переходом на 200 мг 2 раза в сутки. Целекоксиб не применяется после аортокоронарного шунтирования, при клинических проявлениях ишемической болезни сердца, перемежающейся хромоте, после перенесенного инсульта.
Противопоказания для назначения системных НПВП (подробнее в Приложении 3):
- высокий риск кардиоваскулярных осложнений;
- язва или эрозии желудочно-кишечного тракта (по результатам эндоскопического исследования);
- хроническая болезнь почек при СКФ
- воспалительные заболевания кишки (язвенный колит, болезнь Крона);
- аллергия на НПВП;
- беременность.
Во всех случаях пользоваться утвержденной инструкцией по применению конкретного препарата.
Комбинирование НПВП с нейротропными витаминами
Нейротропные витамины стимулируют процессы, улучшающие функцию нервной системы и уменьшающие болевой синдром. В частности, витамин В1 улучшает энергообеспечение нейронов, витамин В6 контролирует синтез транспортных белков в осевых цилиндрах, витамин В12 активирует синтез липопротеинов, служащих структурным элементом миелиновых волокон. Комплекс витаминов В1, В6, В12 тормозит прохождение болевых импульсов не только на уровне заднего рога, но и в таламусе.
Во многих исследованиях подтверждено потенцирующее действие витаминов группы В при болях в спине при применении НПВП.
В последние годы стали активно применяться трехкомпонентные комплексы, содержащие В1 (тиамин), В6 (пиридоксин) и В12 (цианокобаламин) в высоких дозах в одной таблетке или ампуле. Примером комбинации такого рода является препарат Нейробион. Используется ступенчатая терапия: сначала инъекционная форма (1 амп./сут) до снятия острых симптомов, далее пероральный прием по 1 табл. 3 раза в день.
Миорелаксанты
При наличии признаков выраженного мышечного спазма и неэффективности монотерапии НПВП рекомендованы миорелаксанты. Назначаются короткими курсами (на 7–14 дней). Среди миорелаксантов используются тизанидин, обладающий центральным миорелаксирующим и анальгезирующим действием, а также толперизон, у которого механизм действия реализуется за счет подавления рефлекторной активности на уровне спинного мозга.
Лекарственный формуляр приведен в Приложении 4.
НЕЛЕКАРСТВЕННЫЕ МЕТОДЫ
Острая неспецифическая боль
Информирование пациента о доброкачественном характере заболевания и высокой вероятности быстрого выздоровления при соблюдении рекомендаций врача. Постельный режим не показан; в тех случаях, когда пациенты вследствие интенсивной боли вынуждены лежать, продолжительность постельного режима не должна превышать 2 дней. Нет оснований рекомендовать пациентам с болью в спине спать на жесткой поверхности. Избегать как чрезмерной двигательной и физической активности, так и длительных статических нагрузок.
Привлечение других специалистов (кинезотерапевта, психолога и др.) осуществляет невролог.
Аркадий Львович Вёрткин, д.м.н., профессор, зав. кафедрой терапии, клинической фармакологии и скорой медицинской помощи Московского государственного медико-стоматологического университета (МГМСУ)
им. А.И. Евдокимова Минздрава России, Москва
Андрей Евгеньевич Каратеев, д.м.н., профессор, зав. лабораторией гастроэнтерологических проблем при ревматических заболеваниях Научно-исследовательского института ревматологии (ФГБНУ НИИР) им. В.А. Насоновой, Москва
Михаил Львович Кукушкин, д.м.н., профессор, зав. лабораторией патофизиологии боли Научно-исследовательского института общей патологии и патофизиологии РАН, Москва
Владимир Анатольевич Парфёнов, д.м.н., профессор, зав. кафедрой нервных болезней и нейрохирурги Первого московского Государственного медицинского Университета (ПМГМУ) им. И.М. Сеченова, Москва
Николай Николаевич Яхно, д.м.н., профессор, академик РАН, профессор кафедры нервных болезней лечебного факультета Первого московского государственного медицинского университета (ПМГМУ) им. И.М. Сеченова, Москва
Герман Юрьевич Кнорринг, к.м.н., доцент кафедры терапии, клинической фармакологии и скорой медицинской помощи Московского государственного медико-стоматологического университета (МГМСУ) им. А.И. Евдокимова Минздрава России, Москва
Анатолий Иванович Мартынов, д.м.н., профессор, академик РАН, профессор кафедры госпитальной терапии № 1 Московского государственного медико-стоматологического университета (МГМСУ) им. А.И. Евдокимова Минздрава России, Москва
Источник
