Постлучевые изменения в позвоночнике
В.С. Шевченко, НИИ онкологии АМН Украины, г. Киев
Международный неврологический журнал 4(20) 2008 / Практикующему неврологу /To Practicing Neurologist/
Лучевая терапия в различных ее модификациях является одним из ведущих методов лечения в онкологии. Несмотря на высокую эффективность и отсутствие альтернативы в некоторых случаях, актуальной остается проблема негативных ее последствий — фиброза, лучевых ожогов кожи и слизистых, угнетения костномозгового кроветворения и пр. Наиболее распространенными осложнениями лучевой терапии являются поражения нервной системы — плекситы, невриты различных локализаций [1, 2]. Ниже приводится описание клинического случая хронической постлучевой миелопатии под маской вторичной интоксикационной полиневропатии.
Больной В., 1964 года рождения, житель Одесской области, поступил в отделение опухолей головы и шеи НИИ онкологии АМН Украины в декабре 2006 года с диагнозом: рак корня языка T2N0M0, стадия ІІ, клиническая группа ІІ. Диагноз верифицирован цитологически — плоскоклеточная карцинома. Получал химиолучевую терапию, суммарная доза облучения составила 60 Гр по расщепленной методике в 2 этапа по 30 Гр с интервалом 4 недели, последний курс облучения — в марте 2007 г.
С сентября 2007 года больной отмечает появление жалоб на слабость в ногах, шаткость при ходьбе, недержание мочи и кала. По месту жительства осмотрен онкологом, невропатологом, урологом, проктологом, обследован (компьютерная томография органов грудной полости, рентгенография пояснично-крестцового отдела позвоночника, ультразвуковое исследование органов брюшной полости и малого таза, ирригография). В результате проведенного обследования данных о пролонгации основного заболевания не получено. Для дальнейшего обследования и лечения направлен повторно в НИИ онкологии АМН Украины с предварительным диагнозом: рак корня языка, Т2N0M0, стадия II, клиническая группа ІІ, состояние после химиолучевой терапии, вторичная интоксикационная полиневропатия.
При поступлении в ноябре 2007 года консультирован неврологом. Предъявляет жалобы на выраженную слабость в руках и ногах, боли в шейном отделе позвоночника, периодически возникающие судороги в ногах, шаткость при ходьбе с тенденцией к падению, недержание мочи и кала. Общее состояние больного на момент осмотра оценено как тяжелое, сознание ясное, контактен, адекватен, ориентирован во времени и пространстве. В неврологическом статусе: со стороны черепно-мозговых нервов очевидной патологии не выявлено. Глубокие рефлексы с рук и ног повышены симметрично, определяются патологические стопные знаки сгибательной и разгибательной групп с обеих сторон. Гипестезия с уровня Th5 по проводниковому типу. Глубокая чувствительность не нарушена. Мышечная сила в руках и ногах снижена до 3–3,5 балла. Мышечный тонус симметрично повышен по пирамидному типу. Верхнюю и нижнюю пробы Барре выполняет с выраженной дисметрией, мимопопаданием с обеих сторон. В позе Ромберга — шаткость с тенденцией к падению. Менингеальный симптомокомплекс не убедителен. Функция тазовых органов нарушена по центральному типу (недержание мочи и кала).
МРТ шейного отдела позвоночника с внутривенным усилением: с уровня С2 по Th1 определяется тотальное снижение плотности вещества спинного мозга без компрессии спинномозгового канала (рис. 1), что с учетом анамнеза расценено как постлучевая миелопатия. Костнодеструктивных изменений не обнаружено.
После проведенного дообследования установлен диагноз: хроническая постлучевая миелопатия шейного отдела.
Больному назначена комплексная терапия с применением противоотечных, антихолинэстеразных препаратов, дезагрегантов. Со слабо положительной динамикой пациент выписан под наблюдение онколога и невропатолога по месту жительства.
Описанный случай свидетельствует о необходимости проведения дифференциальной диагностики при клинических признаках поражения спинного мозга у онкологических больных.
Источник
Лучевая диагностика постлучевых изменений костного мозга
а) Определения:
• Трансформация на фоне лучевой терапии красного костного мозга в жировой
б) Визуализация:
1. Общие характеристики:
• Наиболее значимый диагностический признак:
о Интенсивность сигнала (ИС) костного мозга в пределах зоны облучения в Т1-режиме соответствует ИС подкожной клетчатки
• Локализация:
о Соответствует области облучения
• Размеры:
о Соответствуют размерам области облучения
• Морфология:
о Однородная гиперинтенсивность сигнала костного мозга:
– Неоднородный характер сигнала дает основание заподозрить рецидив поражения костного мозга
о Четкие границы между измененным и неизмененным костным мозгом (границы области облучения)
2. Рентгенологические данные постлучевых изменений костного мозга:
• Рентгенография:
о ± остеопения, компрессионные переломы
3. КТ постлучевых изменений костного мозга:
• Костная КТ:
о ± компрессионные переломы
о Неинформативна в отношении диагностики жировой перестройки костного мозга
4. МРТ постлучевых изменений костного мозга:
• Т1-ВИ:
о Очень высокая интенсивность сигнала костного мозга (соответствует жировой ткани)
• Т2-ВИ:
о Промежуточная ИС, соответствует жировой ткани
• PD/промежуточный режимы:
о Промежуточная ИС, соответствует жировой ткани
• STIR:
о Высокая интенсивность сигнала в острую фазу (отек)
о Низкая интенсивность сигнала в последующем (жировая перестройка)
• Т1-ВИ с КУ:
о Контрастное усиление сигнала в острую фазу:
– Возможно связано с застойными явлениями
о В последующем контрастное усиление исчезает:
– Снижение кровоснабжения, фиброз
• Первые три недели:
о Отсутствие изменений или ранняя гиперинтенсивность Т1-сигнала костного мозга:
– Гиперинтенсивность сигнала позволяет предположить наличие кровоизлияний ± жировую перестройку
о Гиперинтенсивность в STIR:
– Отек и некроз костного мозга
– Изменения наиболее выражены в течение первых 9 дней после облучения, в последующем ИС постепенно снижается
• 3-6 недель:
о Неоднородный пятнистый характер сигнала в Т1
о Усиление сигнала за счет жировой перестройки в центральных отделах тел позвонков вокруг базивертебральных вен
• После шести недель:
о Диффузная и гомогенная гиперинтенсивность сигнала в Т1
о Полосы промежуточной ИС по периферии:
– Вокруг центрального гиперинтенсивного костного мозга
– Могут быть отражением регенерации гемопоэтического костного мозга
о Характерные изменения, захватывающие >90% костного мозга в пределах области облучения
5. Радиоизотопные исследования:
• Костная сцинтиграфия:
о Четко ограниченное очаговое или диффузное снижение захвата изотопа вследствие уменьшения кровоснабжения облученных участков костного мозга
• ПЭТ:
о Снижение метаболической активности костного мозга
• Сцинтиграфия с серным коллоидом, меченым 99mТс:
о Четко ограниченная «холодная» зона, соответствующая границам области облучения
6. Другие методы исследования:
• Двухэнергетическая рентгеновская абсорбциометрия:
о Возможно уменьшение костной массы
7. Рекомендации по визуализации:
• Наиболее оптимальный метод диагностики:
о Методом выбора при исследовании костного мозга является МРТ
• Протокол исследования:
о Т1-ВИ — наиболее чувствительный в отношении диагностики жировой перестройки костного мозга режим
о STIR или FSET1 с насыщением жировой ткани наиболее информативны в отношении диагностики рецидивов или остаточных явлений поражений костного мозга
о Т1-ВИ без КУ и с КУ и подавлением сигнала жира увеличивают чувствительность в отношении диагностики очаговых поражений
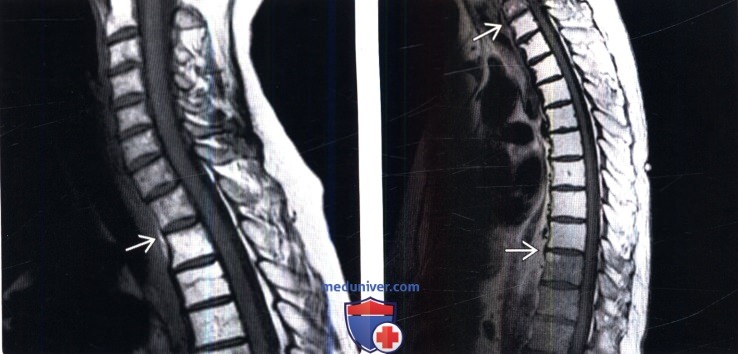
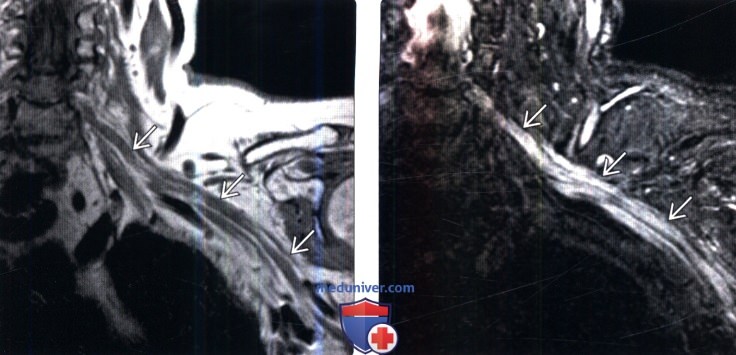
(Слева) Сагиттальный срез, Т1-ВИ шейно-грудного отдела позвоночника: признаки однородного усиления сигнала костного мозга грудных позвонков с достаточно хорошо выраженной переходной зоной этих изменений на уровне Т1-Т2, т. е. на уровне верхней границы области облучения.
(Справа) Сагиттальное Т1-ВИ с признаками гомогенной постлучевой жировой перестройки костного мозга грудных позвонков и четкими границами этих изменений, соответствующими границам области облучения.
в) Дифференциальная диагностика постлучевых изменений костного мозга:
1. Нормальный жировой костный мозг:
• Изменения коррелируют с возрастом пациента
• Преимущественная интенсивность сигнала соответствует жировой ткани, нередка некоторая неоднородность сигнала
• Отсутствие четких границ с неизмененным костным мозгом
• ± компрессионные переломы
• Отсутствие патологических изменений захвата изотопов при сцинтиграфии и ПЭТ
2. Гемангиома позвонка:
• Четко ограниченное округлое образование
• Типична гиперинтенсивность в Т1 и Т2, связанная с наличием жировой стромы
• Яркое контрастное усиление
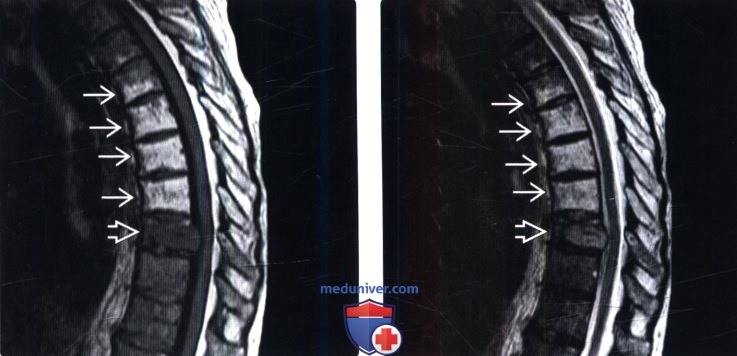
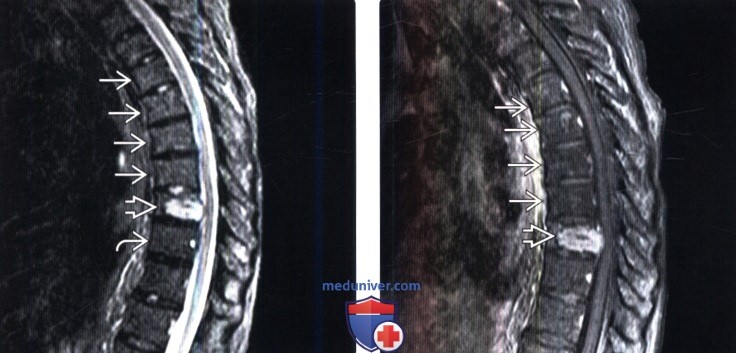
(Слева) На сагиттальном Т1-ВИ определяются признаки жировой перестройки костного мозга нижней половины тела Т5 и целиком тел и задних элементов Т6-Т8 позвонков. Обратите внимание на T9 позвонок, костный мозг которого практически полностью инфильтрирован опухолью.
(Справа) Сагиттальный срез, Т2-ВИ: признаки жировой перестройки костного мозга нижней половины тела Т5 и целиком тел и задних элементов Т6-Т8 позвонков. Костный мозг T9 позвонка инфильтрирован метастазом опухоли.
г) Патология:
1. Общие характеристики:
• Этиология:
о Лучевое повреждение гемопоэтических элементов костного мозга (отличающихся высокой радиочувствительностью)
о Сопутствующее снижение костной массы
о Изменения МР-сигнала костного мозга зависят от дозы облучения, ее фракционирования и времени, прошедшего с момента окончания терапии:
– Признаки жировой перестройки костного мозга появляются через две недели после облучения:
Через два месяца после облучения жировая перестройка наблюдается более, чем у 90% пациентов
– При дозе облучения 1,25 Гр ИС костного мозга не меняется
– При дозе в 50 Гр признаки жировой перестройки сохраняются и через девять лет после облучения:
Полное и необратимое исчезновение гемопоэтических элементов
– При дозах 20-30 Гр через 10 лет восстанавливается картина нормального костного мозга:
Частичное восстановление наступает в период от 2 до 9 лет
о Реконверсия жирового костного мозга в красный у детей наступает через 11-30 месяцев после облучения
• Генетика:
о Генетическая предрасположенность отсутствует
• Сочетанные изменения:
о Остеопения
о Остеопоротические компрессионные переломы
о Остеонекроз:
– Четкая граница между нормальным костным мозгом и зоной инфаркта
– МРТ:
Гиперинтенсивность в STIR и FS Т2
Гипоинтенсивность в Т1
± внутрипозвонковое жидкостное скопление
± КУ после внутривенного введения гадолиния
– Рентгенография, КТ:
± линейное скопление газа в теле позвонка, склероз
– Костная сцинтиграфия:
Отсутствие захвата изотопа, за исключением случаев развития коллапса тела позвонка
Бывает сложно отличить от рецидива метастатического поражения
о Для дифференциальной диагностики показана биопсия
о Рецидив или продолженный рост опухоли:
– Множественные дискретные очаги
– Парадуральный или паравертебральный мягкотканный компонент
– Патологические переломы
– Гипоинтенсивная в Т1 зона, окруженная жировым костным мозгом
– Гиперинтенсивность в STIR или FS Т2
– Очаговые образования после курса лечения могут не накапливать контраст
о Постлучевой миелит:
– Диффузная гиперинтенсивность Т2-сигнала спинного мозга в пределах области облучения
– Умеренная гипоинтенсивность в Т1
– Утолщение спинного мозга ± неправильной формы очаги контрастного усиления (некроз)
2. Микроскопия:
• Исследование на крысах, подвергшихся однократному облучению в дозе 20 Гр
• Снижение числа клеточных элементов и повреждение синусоидных сосудов:
о Сочетанные отек и кровоизлияния
• Восполнение клеточного состава костного мозга:
о Одновременное увеличение и жирового компонента
• Уменьшение клеточности костного мозга и уменьшение числа синусоидов:
о Фиброз с последующим увеличением жирового компонента
• Постепенная регенерация гемопоэтических элементов и синусоидов

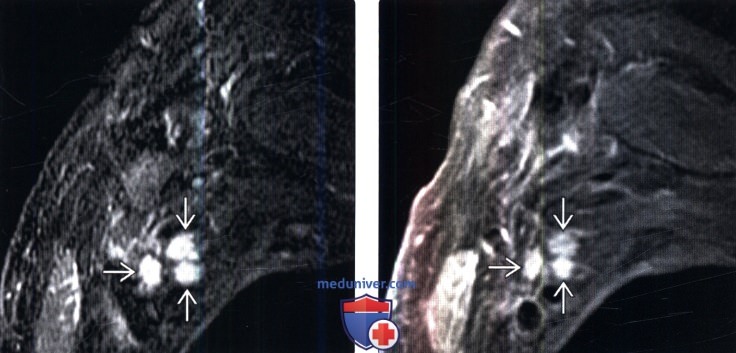
(Слева) На сагиттальном STIR МР-И у этого же пациента видно, что нормальный костный мозг и измененный в результате облучения костный мозг характеризуются практически одинаковой низкой интенсивностью сигнала, тогда как очаг метастатического поражения характеризуется высокой интенсивностью сигнала.
(Справа) На следующем сагиттальном FS T1-ВИ с КУ отмечается подавление сигнала и отсутствие контрастного усиления подвергшегося облучению и последующей жировой перестройке костного мозга нижней половины тела Т5 и тел и задних элементов Т6-Т8 позвонков. Тело T9 позвонка практически полностью замещено накапливающим контраст метастазом опухоли.
д) Клинические особенности:
1. Клиническая картина постлучевых изменений костного мозга:
• Наиболее распространенные симптомы/признаки:
о Обычно бессимптомное течение
• Другие симптомы/признаки:
о Боль (перелом)
о Миелопатия или радикулопатия вследствие компрессионного перелома или инфильтрации опухолью
• Особенности клинической картины:
о Развитие или прогрессирование болевого синдрома и неврологического дефицита обычно связано с постлучевым некрозом, переломами позвонков или рецидивом/прогрессирова-нием опухоли
2. Демография:
• Возраст:
о Дети и взрослые
• Пол:
о М = Ж
• Этническая предрасположенность:
о Отсутствует
• Эпидемиология:
о Ожидаемая находка у всех пациентов, подвергшихся лучевой терапии
3. Течение заболевания и прогноз:
• Восстановление картины нормального костного мозга при длительных сроках наблюдения за пациентами: > 10 лет
• Зависят в первую очередь от характера первичного заболевания, по поводу которого проводилась лучевая терапия
4. Лечение постлучевых изменений костного мозга:
• Ожидаемая находка после проведенной лучевой терапии, при отсутствии осложнений лечения не требует:
о Симптоматическая терапия при компрессионных переломах
о Хирургическое лечение при сдавлении спинного мозга или нестабильности позвоночника
е) Диагностическая памятка:
1. Следует учесть:
• Методом выбора при исследовании костного мозга является МРТ: Т2-ВИ FS или STIR и Т1 FS с КУ
2. Советы по интерпретации изображений:
• Гомогенная жировая перестройка костного мозга, четко отграниченная от неизмененного костного мозга, является характерным диагностическим признаком постлучевых изменений костного мозга
ж) Список использованной литературы:
1. Carmona R et al: Fat composition changes in bone marrow during chemotherapy and radiation therapy. Int J Radiat Oncol Biol Phys. 90(1):1 55-63, 2014
2. Bolan PJ et al: Water-fat MRI for assessing changes in bone marrow composition due to radiation and chemotherapy in gynecologic cancer patients. J Magn Reson Imaging. 38(6): 1578-84, 2013
3. Hwang S et al: Magnetic resonance imaging of bone marrow in oncology. Part 2. Skeletal Radiol. 36(11):1017-27, 2007
4. Tall MA et al: MR imaging of the spinal bone marrow. Magn Reson Imaging Clin N Am. 15(2): 1 75-98, vi, 2007
5. Foster К et al: MRI of the marrow in the paediatric skeleton. Clin Radiol. 59(8):651-73, 2004
6. Shih WJ et al: Tc-99m depreotide SPECT demonstrates photon-deficiency in the thoracic vertebrae after adjunct radiation therapy of lung cancer: correlation with MRI and bone scintigraphy. Ann Nucl Med. 17(3):245-8, 2003
7. Otake S et al: Radiation-induced changes in MR signal intensity and contrast enhancement of lumbosacral vertebrae: do changes occur only inside the radiation therapy field? Radiology. 222(1): 179-83, 2002
8. Onu M et al: Early MR changes in vertebral bone marrow for patients following radiotherapy. Eur Radiol. 11 (8): 1463-9, 2001
– Также рекомендуем “МРТ при передней поясничной радикулопатии”
Редактор: Искандер Милевски. Дата публикации: 20.9.2019
Источник
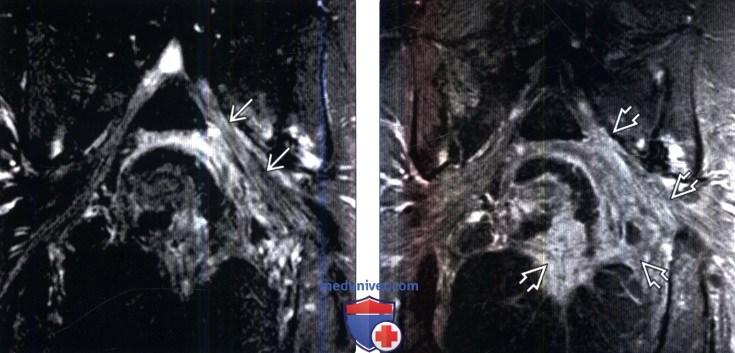
Лучевая диагностика постлучевой плексопатииа) Терминология: б) Визуализация: 1. Общие характеристики: 2. КТ при постлучевой плексопатии: 3. МРТ при постлучевой плексопатии: 4. Радиоизотопные исследования: 5. Другие методы исследования: 6. Рекомендации по визуализации:
в) Дифференциальная диагностика постлучевой плексопатии: 1. Инфильтрация плечевого сплетения злокачественной опухолью: 2. Плексиформная нейрофиброма: 3. Тракционное повреждение плечевого сплетения:
г) Патология: 1. Общие характеристики: 2. Стадирование, степени и классификация постлучевой плексопатии: 3. Макроскопические и хирургические особенности: 4. Микроскопия:
д) Клинические особенности: 1. Клиническая картина: 2. Демография: 3. Течение заболевания и прогноз: 4. Лечение постлучевого плексита: е) Диагностическая памятка: ж) Список использованной литературы: – Также рекомендуем “МРТ при опухоли оболочки периферического нерва” Редактор: Искандер Милевски. Дата публикации: 11.9.2019 |
Источник