Новые технологии в лечении травм позвоночника

Наука часто апеллирует к интуитивной прозорливости. Прорывы в медицине иногда происходят из слухов и легенд (Эдвард Дженнер слышал, что доярки, инфицированные коровьей оспой, не болеют оспой – так и появилась первая вакцинация от оспы); от случайного заражения экспериментального материала (открытие пенициллина и неопрена); и от неожиданных побочных эффектов лекарств (Виагра изначально предназначалась для лечения заболеваний сердца).
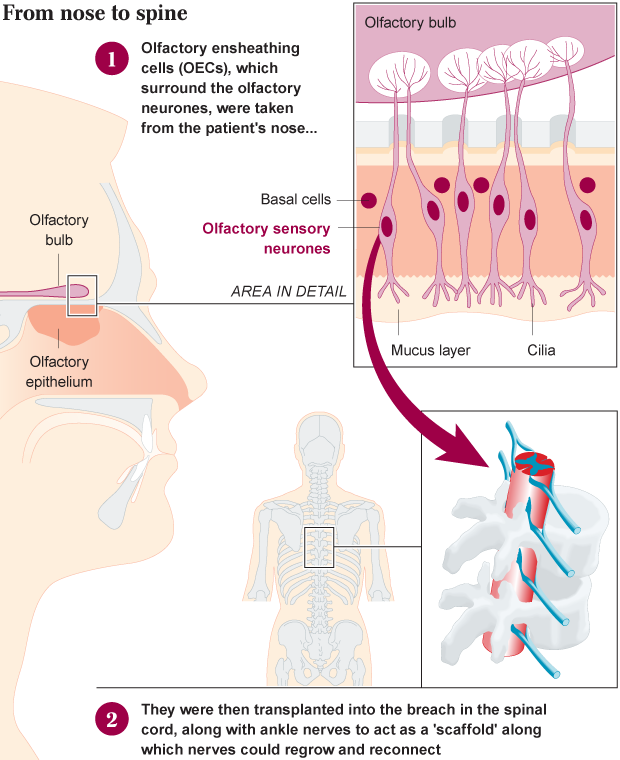
И мог ли предполагать Дарек Фидика , 38-летний польский пожарный, болеющий синуситом, что попадет в историю медицины как первый парализованный больной, который стал ходить после трансплантации нервных клеток. Восстановление движений в ногах дало пациенту невероятные ощущения и стало фактически вторым рождением. У пациента Фидика спинной мозг был полностью перерезан ножом во время драки с бывшим мужем жены, и Фидика согласился на пересадку клеток, полученных из носа. Клетки, которые называются обонятельные оболочечные (глиальные) клетки , как известно, влияют на регенерацию обонятельных нервов, которые транспортируют сигналы с обонятельных рецепторов в мозг и восстанавливаются каждые 30 дней.
В экспериментах на крысах и собаках, применение этих клеток было обещающим и они служили в качестве «мостика», который можно использовать для того, чтобы восстановить разорванные нервы; ранее парализованные животные после трансплантации этих клеток восстанавливали способность двигаться. Различные группы ученых по всему миру начали экспериментировать для внедрения этой методики для лечения парализованных людей. Но польский хирург Фидика был вынужден применить особенно смелый подход; слизистая оболочка Фидика была фактически разрушена хроническим аллергическим синуситом и это означало, что клетки ООК не могут быть получены из носовых ходов.
Вместо этих специальных клеток, – которые не являются стволовыми клетками, а взрослыми функционирующими клетками – были получены нервные клетки с помощью операции на головном мозге. Нейрохирурги в университетской больнице Вроцлава в Польше проникли в череп Фидика, экстрагировали левую обонятельную луковицу и подготовили готовую к трансплантации культуру клеток ООК. Эти культивированные клетки затем пересадили в спинной мозг в область разрыва, вместе с полосками нервов лодыжки, чтобы задействовать их в качестве каркаса, по которому нервы могли бы вырасти.
В течение полутора лет появились результаты новаторской операции: пожарный, который также получал физиотерапию, ЛФК, смог частично перемещать свои нижние конечности, появились ощущения в ногах, выросли мышцы на левом бедре и в некоторой степени восстановились функции мочевого пузыря и кишечника, а также половые функции.
При таких тяжелых травмах спинного мозга как у Фидика (класса А), как правило, пациенты остаются парализованными на всю жизнь. Благодаря этому революционному вмешательству пациент стал передвигаться с помощью ходунков, и тяжесть его состояния перешла в класс С., Кроме того, как ни удивительно, он не потерял обоняние.
Операция была проведена в Польше, но была провозглашена в качестве прорыва британской медицины, так как проводилась под руководством профессора Джеффри Райзмана, из отделения нейрохирургии Университетского колледжа неврологии Лондона Профессор Райзман заявил. “Я считаю, что мы стоим на пороге исторического переломного момента в медицине “
В финансировании также участвовали UK Stem Cell Foundation и Nicholls Spinal Injury Foundation.NSIF это благотворительный британский фонд, который был создан Дэвидом Николсом, чей сын Дэниел был парализован после травмы позвоночника во время купания. Организация Spinal Injuries Association встретила известие о проведенной успешной операции с “осторожным оптимизмом”, так как в настоящее время в Великобритании почти 40 000 человек с травмой спинного мозга.
Профессор Райзман еще в 1985 году исследовал клетки ООК и в 1997 году показал , что они могут повернуть вспять паралич у крыс. Теперь же свидетельствует Кевин Шейксшеф, профессор инженерии тканей из Университета Ноттингема, настойчивость стала давать плоды. “Это успех не в одночасье ,” говорит профессор Shakesheff, который сотрудничал с профессором Райзманом в начале девяностых. “Джефф достиг таких блестящих результатов длительной работой в течение последних 20 лет, и он наблюдал за клиническими исследованиями в течение последнего десятилетия. Он знает о ООК больше, чем кто-либо в мире “.
Несмотря на то, что периферическая нервная система, в конечностях, может самовосстанавливаться – порезка пальца кухонным ножом, например, не будет, как правило, приводить к необратимому повреждению – то же самое не возникает при повреждении спинного мозга. Этот огромное слепое пятно в системе регенерации организма стало мотивацией для многих тысяч ученых, работающих в области регенерации тканей. Также интерес к регенерации спинного мозга стимулировал сбор средств для проведения научных изысканий: Фонд Кристофера и Дана Рив был организован после того, как актер, сыгравший последнего Супермена, был парализован после травмы во время верховой езды и этот фонд за короткое время собрал более $ 110 млн.
Мало того, что исследования могут помочь спинальным больным, но они имеют и долгосрочные цели: болезни старения, такие как заболевания сердца, рак и болезнь Паркинсона, являются в значительной степени результатом дегенерации и гибели клеток. Возможность создания здоровых клеток, которыми можно заменить старые клетки, очевидно, будет приоритетом медицины в ближайшем будущем.
В последние десять лет надежда восстановления тканей, в том числе и регенерации нервов, в значительной степени подогревалась ажиотажем вокруг стволовых клеток. Стволовые клетки делятся на два типа: эмбриональные – те, что могут быть собраны из ранних эмбрионов, со всеми вытекающими этическими проблемами; и взрослые стволовые клеток, которые могут быть извлечены из костного мозга и некоторых других тканей организма взрослого.
Ключевой особенностью стволовых клеток является их потенциальная возможность превращаться в определенные типы клеток; и давняя мечта ученых разблокировать этот потенциал так, чтобы он был аналогичен потенциалу эмбриональных клеток, который гораздо выше.
Именно невысокий потенциал взрослых стволовых клеток был причиной многочисленных неудачных клинических испытаний применения их для лечения сердечно-сосудистых заболеваний, диабета, болезни Паркинсона и травм спинного мозга.
В отличие от этого, ООК являются не стволовыми клетками, а взрослыми клетками, которые уже имеют окончательную специализизацию. Но именно их окончательная функция – как-то обучать и стимулировать рост нервных клеток в носовых ходах – была успешно использована в проведенном клиническом эксперименте.
 Но наука все еще далека от полного лечения травм спинного мозга. Фидику повезло, и он больше не прикован к инвалидной коляске и через некоторое время сможет жить полноценно. Его восстановление, отчет о которых был опубликован в журнале трансплантации журнал Cell, может быть обусловлено целым рядом факторов. Его спинной мозг был разрезан относительно чисто; что, возможно, облегчило растущим нервным клеткам, преодолеть зазор в8 мм. У большинства же пациентов травмы спинного мозга гораздо более сложные .
Но наука все еще далека от полного лечения травм спинного мозга. Фидику повезло, и он больше не прикован к инвалидной коляске и через некоторое время сможет жить полноценно. Его восстановление, отчет о которых был опубликован в журнале трансплантации журнал Cell, может быть обусловлено целым рядом факторов. Его спинной мозг был разрезан относительно чисто; что, возможно, облегчило растущим нервным клеткам, преодолеть зазор в8 мм. У большинства же пациентов травмы спинного мозга гораздо более сложные .
Вполне возможно, что у хирурга было достаточное количество ООК клеток и ему удалось ввести их в нужное место. Для того чтобы убедиться в реальной эффективности такой методики лечения, необходимо провести ряд исследований на достаточно большой группе пациентов, и только затем можно говорить о реальной эффективности методики.
Но прорывы когда- то должны начинаться. Дэвид Николс потратил почти миллион фунтов на фундаментальные медицинские исследования, которые могли бы помочь его парализованному сыну Даниилу. Николс был предупрежден врачами, не предаваться ложным надеждам. Не испугавшись, он передал деньги, которые он собрал, профессору Райзману со словами: «Все говорили, я теряю время, но что такое жизнь без надежды?”
Профессор Райзман, обнадежил своего спонсора и сделал именно то, что делают ученые экспериментаторы: он следовал за наукой везде, куда она приводила, несмотря на обескураживающие трудности. Он сделал очень простой научный расчет- это то, что врачи могли изъять клетки из одной части тела, вставить их в другую часть тела, и те же клетки могут просто выполнять свою обычную работу. Если такое работает у крыс и собак; кто скажет, что это не может работать в организме человека?
В некотором смысле, такие медицинские прорывы фактически связаны с обычной механикой: мы не неприкосновенные организмы, а лишь «мешок с клетками». Но то, что парализованный человек восстановил способность ходить за счет передислокации собственных обонятельных клеток, является доказательством того, что человеческий организм еще более примечательный и удивительный, чем мы могли представить…
Источник
«Это потрясающее чувство. Я вновь могу согнуть колени, самостоятельно поднять ноги и даже пошевелить пальцами», — рассказывает один из участников экспериментального лечения, которому удалось вернуть свои двигательные способности за счет технологии спинномозговой стимуляции. После травмы позвоночника, полученной 2010 году, его ноги были парализованы.
Фактически сразу несколько исследовательских групп как в России, так и за рубежом трудятся над различными способами лечения паралича, вызванного инсультом или травмой спинного мозга. Благодаря инновационным протоколам лечения пациенты с хронической параплегией заново учатся ходить.
Подобные технологии позволяют стимулировать спинной мозг сверхточными электрическими импульсами, активировать нейромышечные связи ниже травмы и одновременно с этим усиливать остаточные команды от мозга.
Какие механизмы реабилитации уже существуют и могут быть использованы для лечения?
Травма спинного мозга приводит к серьезным нарушениям двигательной активности, значительно снижает качество жизни и влечет за собой значительные расходы для семей и общества. Чтобы преодолеть последствия подобных недугов, ученые стараются восстановить у парализованных людей именно способность ходить.
По мнению нейрофизиологов решающее значение для реабилитации двигательных функций имеет временное совпадение между внешней электостимуляцией и остаточной командой мозга. Так, чтобы добиться идеальной синхронизации, швейцарские ученые из Федеральной политехнической школы Лозанны (EPFL) связали расшифровку двигательного намерения мозга с подачей электросигналов для стимуляции спинного мозга через имплант.
В России подобными исследованиями занимается команда Юрия Герасименко, который много лет возглавляет Институт физиологии им. И.П. Павлова в Санкт-Петербурге. Совместно с российскими и американскими коллегами ему удалось сломать главный стереотип о параличе нижних конечностей.
Ещё лет двадцать назад считалось, что повреждения позвоночника носят анатомический характер, а движениями ног напрямую управляет головной мозг. Ученые расценивали позвоночник исключительно как проводником между мозгом и нижними конечностями и если под воздействием травмы эта связь нарушалась, то человек был вынужден навсегда пересесть в инвалидное кресло.
Но это оказалось заблуждением.
В Институте физиологии после долгих лет упорной работы сумели доказать, что учёные прошлых лет недооценивали значимость спинного мозга, и за движения нижних конечностей человека, в частности, способность ходить, отвечает именно спинной мозг.
Спинной мозг – орган центральной нервной системы, нервная трубка, находящаяся в позвоночном канале. Она делится на 31 сегмент, каждый из которых управляет своей частью тела и собирает информацию – болевую, кожную и мышечную.
Спинной мозг обладает всеми механизмами для инициации и регуляции движений. А это значит, что «починить» человека при параличе можно воздействуя именно на этот орган. Задачей ученых, работающих в Институте физиологии, было научиться управлять шагами, стимулируя спинной мозг. Нейрофизиологи проводили тестирование различных участков спинного мозга у животных в продольном и горизонтальном направлении, пока, наконец, не нашли зону, стимуляция которой вызывала шагательные движения.
«У человека, как у любого млекопитающего в спинном мозгу существуют участки, ответственные за ходьбу. В Хьюстоне поставили задачу – применить к пациентам с травмой спинного мозга стимуляцию, чтобы инициировать шагательные движения. И мы описали у всех пациентов зону, стимуляция которой вызывает необходимую реакцию», – рассказывает Юрий Герасименко.
В ходе дальнейшей работы учёным удалось доказать, что поражение спинного мозга, возникающее при травме позвоночника, носит не анатомический характер, а функциональный. Следовательно, воздействуя на определенные центры, можно восстановить функцию, нарушенную травмой.
Команда Юрия Герасименко разработала такую методику воздействия на спинной мозга, в ходе которой на оболочку нервной трубки устанавливаются электроды, а под брюшину имплантируется стимулятор. Вследствие электростимуляции нервные клетки, взаимодействуя с проводящим имплантом, создают связанные цепочки в обход повреждённого участка и организм «ремонтирует» систему связи между головным и спинным мозгом.
По итогам такого лечения пациент восстанавливается от полного паралича до возможности самостоятельно ходить своими ногами. Стимулятор подает электрические импульсы, которые запускают парализованные ноги и одновременно с этим сигналы «эхом» уходят в головной мозг. И понемногу, шаг за шагом, человек заново учится управлять телом.
«Я даже сидеть стал намного лучше, потому что окреп позвоночник. Я стреляю из лука, хожу по беговой дорожке. Да, мне пока нужны ходунки, и за мной присматривает тренер, но я уверен, что скоро не буду нуждаться в помощи. Это главное для меня», – рассказал один из пациентов доктора Герасименко.
В тоже время, европейские ученые смогли далеко продвинуться в вопросе эффективности и скорости лечения. Если раньше пациенты демонстрировали прогресс только спустя несколько месяцев интенсивной реабилитации, чаще всего — примерно через год. То исследование, выполненное в Швейцарии, показало, как пациенты смогли вновь ходить (с небольшой помощью) спустя всего несколько дней. А после нескольких месяцев тренировок контролировать ранее парализованные мышцы ног даже при отсутствии электростимуляции.
Разница подходов заключалась в том, насколько постоянным был внешний источник тока. Для эпидуральной электростимуляции, как в других исследованиях, пациенту было имплантировано устройство, которое доставляет электрические сигналы в позвоночный столб ниже области повреждений. Когда травма нарушает связь между спинным и головным мозгом, не давая нервным сигналам достигать конечностей, электростимулятор выступает в роли «моста», перенося электрические сигналы в области позвоночника под местом травмы.
Чтобы понять, как нервная система подает электрические сигналы, чтобы обеспечить каждое движение конечностей, исследователи создали «карту» того, как выглядят типичные импульсы мозга, направленные на активацию движений. Затем они определили, в какую область позвоночника электроды должны доставлять стимулирующие сигналы, чтобы соответствовать обнаруженным паттернам и построили систему, которая передавала сигналы ровно туда, куда нужно.
Ученым пришлось подбирать отдельные параметры системы под каждого пациента. Они даже создали персонализированные модели позвоночников, находящиеся в солевом растворе, проводящем электрический ток, что позволило команде в точности определить, куда поместить электроды при последующей операции. Затем паттерны электрических сигналов были откалиброваны под каждого пациента.
«Все подопытные смогли ходить с использованием ассистивных устройств спустя неделю», — подтвердила одна из руководителей группы ученых Джоселин Блотч. В последующих тестах пациенты оказались способны произвольно выбирать длину и скорость своих шагов и в течении часа идти по беговой дорожке, проходя дистанцию порядка одного километра. Все движения самостоятельно выбирались человеком, а эпидуральный имплант при этом не генерировал никаких непроизвольных движений.
«Наши пациенты должны были постоянно думать о совершении подходящих движений ног. Их мозг оставался активным все время, чтобы отрабатывать сигналы цепи обратной связи с электростимуляцией, которая активировала мышцы», — сказала Карен Минассиан, одна из авторов работы. Из-за постоянной вовлеченности, лечение привело к тому, что произвольные движения со временем восстанавливались по мере того, как вновь появлялись соединения в нервной системе.
Успешность лечения зависит от ряда факторов, включая тяжесть травмы и уровень оставшихся двигательных функций. Для некоторых, оно может привести к масштабным улучшениям за короткое время. По мнению ученых, проверка методики на большем числе подопытных станет важным следующим шагом. Ученые планируют изучить результаты методики на людях, получивших свои травмы недавно, когда «потенциал пластичности находится на максимальном уровне, а нейромышечная система еще не испытала эффекта атрофии вследствие хронического паралича».
Ученые отмечают, что данная техника пока еще не готова для применения в клинических условиях. Необходимо тщательно проверить все аспекты подобного лечения, в том числе его эффект на повседневную жизнь пациента за пределами госпиталя. Исследователи разработали активируемую голосом систему, которая позволяет пациенту включать и выключать эпидуральную электростимуляцию по желанию, а также выбирать один из нескольких режимов стимуляции: ходьба, езда на трицикле и т.д. Заставить имплант работать — это важная задача, но также необходимо сделать его доступной использования пациентом в повседневных условиях.
Уже сейчас российские учёные создали следующее поколение подобного устройства – беспроводной стимулятор. Эти открытия и разработки лягут в основу новых интернациональных проектов, которые построят будущее медицинской реабилитации. Будущее, в котором людям не понадобятся инвалидные коляски.
Источник
Препарат на основе двух генов поможет восстановить двигательную активность пациента после травмы спинного мозга. Революционная разработка российских ученых защищает нейроны от гибели, стимулирует рост кровеносных сосудов и новых нервных волокон. Эффективность препарата показали проведенные на крысах эксперименты — спустя несколько месяцев после начала лечения животные смогли ходить на прежде парализованных конечностях. Для того чтобы начать доклинические испытания, исследователям осталось решить проблемы с финансированием.
Предотвратить рубцевание
Травма спинного мозга, возникшая в результате аварии, несчастного случая или падения с высоты, нередко приводит к потере чувствительности и способности двигать частями тела ниже места поражения. Сейчас помочь мышцам усилить сигнал может только экзоскелет и нейропротезы, и то при условии, что не полностью утрачена связь между спинным и головным мозгом. Исследователи из Казанского федерального университета (КФУ) создали препарат, который позволяет успешно бороться с травмами спинного мозга, несмотря на наличие осложняющих выздоровление факторов.
Дело в том, что при повреждении спинного мозга организм постепенно наращивает в месте травмы рубец, состоящий из соединительной ткани. Он необходим для своеобразной фиксации места повреждения, но в дальнейшем препятствует росту аксонов, отростков нервных клеток, с помощью которых осуществляется связь с другими клетками.
Перед исследователями стояла задача создать такой препарат, который снижал бы скорость образования рубца и восстанавливал нервную ткань.
Ампула с ДНК
Исследователи из института фундаментальной медицины и биологии КФУ создали такой препарат, взяв за его основу два гена (VEGF и FGF2). Первый ген нормализует кровоснабжение при нейротравме, поддерживает выживаемость нейронов, стимулирует нейрогенез, рост новых сосудов и аксонов. Второй ген представляет собой фактор роста, обладает выраженным нейротрофическим действием — поддерживает выживаемость клеток в области повреждения, способствует развитию нервных волокон. Получившийся препарат содержит и регуляторные элементы, которые контролируют работу этих генов.
— Никаких изменений в ДНК человека не происходит, оба этих гена и так присутствуют в организме человека, — пояснил руководитель лаборатории генных и клеточных технологий института фундаментальной медицины и биологии КФУ Альберт Ризванов. — Мы просто вносим в тело дополнительные копии активных генов, с помощью нескольких микроинъекций в спинной мозг выше и ниже травмы. Тем самым мы модифицируем часть нервных клеток (но не «вмешиваемся» в их ядро) и «программируем» их на усиленный рост и восстановление.
Испытания препарата на животных проходили следующим образом. Чтобы смоделировать повреждение спинного мозга, у подопытных вскрывали позвоночник и по нему с помощью специального молоточка наносили удар строго определенной силы. После операции животные теряли чувствительность задних конечностей и способность ими двигать. Во время всего эксперимента за животными тщательно ухаживали, помогая справляться с гигиеной и приемом пищи.
После нанесения травмы ученые переходили к лечению. Опытной группе животных вводили генный препарат, а контрольной позволяли восстанавливаться без стороннего вмешательства.
Двигай лапами
У крыс контрольной группы через два месяца после травмы наблюдалось частичное восстановление двигательных функций — животные сгибали лапы в одном или двух суставах. Однако полноценно передвигаться, удерживать вес тела и координировать движения грызуны не могли. Крысы в опытной группе в этот же период стали уверенно вставать на лапы, ходить, контролируя движения передних и задних конечностей.
— Помимо применения генного препарата мы проводим исследования эффективности лечения травм спинного мозга с помощью мезенхимных стволовых клеток, — рассказал старший научный сотрудник лаборатории генных и клеточных технологий института фундаментальной медицины и биологии КФУ Яна Мухамедшина. — Результаты обеих работ обнадеживают и показывают, что мы можем эффективно восстанавливать травмированный спинной мозг и его функции у крупных животных, в частности свиней, а в дальнейшем и у человека.
В перспективе ученые планируют сочетать эти методики для лечения травм головного мозга и терапии нейродегенеративных заболеваний.
Несмотря на то что гены в составе препарата и так присутствуют в человеческом организме, некий элемент риска всё равно есть и его невозможно предсказать, считает директор Института молекулярной медицины Научно-технологического парка биомедицины Сеченовского университета Андрей Замятнин.
— В составе генетической конструкции, которая используется, есть части (регуляторные элементы), которые в человеческом организме отсутствуют, — пояснил он. — Их влияние на организм абсолютно непредсказуемо. Поэтому для доказательства безопасности препарата необходимо провести клинические испытания.
Ученые готовы начать доклинические испытания в течение года, если решат вопрос финансирования.
Источник
