Локальная инъекционная терапия позвоночника


Боль –где бы она ни локализовалась и какой бы причиной не была вызвана, причиняет современному человеку физическое и психологическое страдание. Естественное желание –побыстрее избавиться от боли. Однако, это –не так уж и просто. Поэтому современная медицинская наука и практика предлагает множество методов борьбы с болевым синдромом. Это, в основном, большая группа фармакологических средств- препаратов, куда входят различные опиоидные и ненаркотические анальгетики (ан –приставка отрицания, от греч. Algos – боль), противовоспалительные(НПВС), гормональные и даже психотропные препараты.
Однако, как показывает повседневная практика, человек, испытывающий боль, в процессе лечения болевого синдрома приобретает «новые болезни» (гастрит, язву желудка или кишечника, психические эмоциональные расстройства и др.), потому что нерациональное использование обезболивающих средств и необходимость их использования достаточно длительное время, в подавляющем большинстве случаев приводит к развитию осложнений. Так, по данным C. Pasero(США), ежегодно от желудочно-кишечных кровотечений, вызванных применением нестероидных противовоспалительных средств(НПВС), умирают от 3 до 15 тысяч человек.
Основной причиной является –тот факт, что дляэффективного купирования локального очага(места) боли необходимо создать там достаточно высокую концентрацию лечебного препарата. К сожалению, лекарства, доставленные в организм традиционным способом (через рот или нецелевой инъекцией) – прежде чем попасть в эпицентр боли, «растворяются» по всему организму, производя массу побочных нежелательных эффектов, а уж затем, возможно, и облегчают боль.
Недопустимо также и длительно терпеть боль –это вызывает изменения психики (неврозы, раздражительность, депрессии и т.д.) и формирование так называемой «хронической» боли, которая связана с расстройством психической сферы и победитькоторую, впоследствии, очень и очень трудно.
Решение этой актуальной проблемы-максимально точное подведение лечебных лекарственных средств к источнику боли. Быстротанаступления, продолжительность эффекта и безопасность (при квалифицированном выполнении процедуры) – порой вызывает удивление и у самих врачей.
Показания к проведению ЛИТ-лечебной блокады:
Головная и лицевая боль:
- синдром крылонебного узла;
- невралгия тройничного нерва;
- невралгия затылочного нерва;
- головная боль напряжения;
- триггерные точки в лицевой мускулатуре, мышцах височно-нижнечелюстного сустава, синдром нижней косой мышцы головы и др.
Боль в области шейного отдела позвоночника:
- корешковый синдром (протрузии и грыжи межпозвонковых дисков);
- шейный фасет-синдром;
- синдром передней лестничной мышцы;
- синдром мышцы, поднимающей лопатку;
- синдром паравертебральных шейных мышц, разгибателей шейного отдела;
- синдром верхней трапециевидной мышцы (триггерные точки) и др.
Боль в области плеча, плечевого сустава:
- плечелопаточный периартроз(периартрит);
- тендиниты мышц вращающей манжеты плеча;
- импинджмент-синдром;
- тендинит двуглавой мышцы плеча;
- артроз акромиально-ключичного сустава;
- синдром «замороженного» плеча;
- комплексный регионарный болевой синдром;
- субакромиальный бурсит и др.
Боль в области верхней конечности:
- невропатия срединного нерва (синдром запястного(карпального) канала);
- невропатия локтевого нерва (ульнарный туннельный синдром (синдром Гюйона));
- теносиновит да Кервена(лучевой стилоидит);
- стенозирующий тендовагинит сгибателей пальцев (синдром Нотта);
- латеральный эпикондилит («локоть теннисиста»);
- медиальный эпикондилит(«локоть гольфиста») и др.;
Боль в области грудного отдела позвоночника:
- синдром малой грудной мышцы;
- триггерные зоны в разгибателях позвоночника;
- грудной фасет-синдром;
- постгерпетическая невралгия и др.
Боль в области поясничного и тазового отдела позвоночника:
- пояснично-тазовый фасет-синдром;
- корешковый синдром(протрузии и грыжи межпозвонковых дисков);
- синдром грушевидной мышцы;
- синдром ягодичных мышц;
- кокцигодиния(синдром мышц тазового дна) и др
Боль в области нижней конечности:
- трохантерит тазобедренного сустава(вертельный бурсит);
- парестетическая мералгия(синдром) Бернгардта-Рота;
- синдром тарзального канала;
- синдром (невринома) Мортона;
- плантарный фасциит(пяточная шпора) и др.
Процедура ЛИТ(блокады) не рекомендуется при:
- Инфекционных процессах,особенно сопровождающихся температурой;
- Инфекционном поражении тканей в зоне проведения ЛИТ;
- Известных аллергических реакциях на препараты ЛИТ;
- Нарушениях свертываемости крови (в том числе при использовании антикоагулянтов);
- Тяжелых нарушениях ритма и проводимости сердца;
- Декомпенсированном сахарном диабете;
- Нестабильности артериального давления(высокие или низкие значения);
- Психических нарушениях(как органических, так и функциональных);
Необходимо помнить, что лечебная блокада является важным, но не единственно необходимым этапом лечения.
Важно, после стихания болевого синдрома, продолжить уточнение особенностей течения заболевания, восстановительное лечение и профилактику. Чтобы болезнь не возвратилась никогда!
ЗАДАТЬ ВОПРОС ПО ТЕЛЕФОНУ:
+7(4922)37-32-49, +7(906)560 61 10
Если по какой то причине Вы не смогли до нас дозвониться, то воспользуйтесь формой обратной связи ниже или сервисом “ЗАКАЗАТЬ ЗВОНОК” в нижнем правом углу страницы. Мы сразу свяжемся с вами , как только освободимся!
Источник
Локальная инъекционная терапия считается одним из важных компонентов лечения воспалительных и дегенеративных заболеваний суставов, позвоночника и мягких тканей. В статье представлены основные группы лекарственных средств, применяемых для внутрисуставного введения у пациентов с данной патологией, включая глюкокортикостероиды, препараты гиалуроновой кислоты и комплексный биоактивный препарат Алфлутоп. Представлены результаты многочисленных исследований, свидетельствующие о том, что препарат Алфлутоп обладает хондропротективным, противовоспалительным, трофическим действием. Данный препарат характеризуется быстро развивающимся клиническим эффектом, продолжительным периодом последействия (четыре – шесть месяцев), высоким профилем безопасности. Может быть рекомендован для широкого применения в ревматологической, неврологической, терапевтической, травматологической и ортопедической практике.

Таблица 1. Характеристика ГКС, применяемых для локальной инъекционной терапии
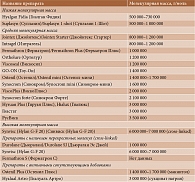
Таблица 2. Препараты гиалуроновой кислоты, применяемые для внутрисуставных инъекций у больных остеоартритом
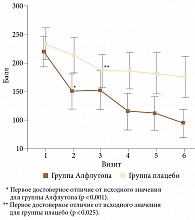
Рис. 1. Динамика интенсивности боли по WOMAC на фоне терапии Алфлутопом или плацебо
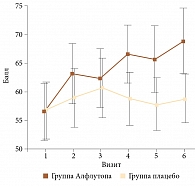
Рис. 2. Динамика Шкалы общего состояния здоровья на фоне терапии Алфлутопом или плацебо
Таблица 3. Динамика маркеров деградации хряща у пациентов с остеоартритом на фоне терапии Алфлутопом и плацебо, нг/ммоль
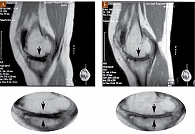
Рис. 3. МРТ коленного сустава пациента К. исходно (А) и через 12 месяцев терапии Алфлутопом (Б)
Cамая частая причина жалоб на боль и нарушение функций опорно-двигательного аппарата – воспаление и дегенеративные изменения структур суставов (гиалиновый хрящ, субхондральная кость). Однако патологический процесс затрагивает не только сустав, но и околосуставные ткани (энтезисы, сухожилия, суставные сумки).
Целями лечения заболеваний опорно-двигательного аппарата являются снижение выраженности симптомов и замедление прогрессирования патологии, что может способствовать улучшению мобильности и качества жизни пациентов.
Один из важных компонентов лечения воспалительных и дегенеративных заболеваний суставов, позвоночника и мягких тканей – локальная инъекционная терапия [1].
В настоящее время эффективность глюкокортикостероидов (ГКС) и препаратов из компонентов матрикса хрящевой ткани для внутрисуставного введения доказана в десятках рандомизированных контролируемых многоцентровых исследований. Поэтому они рекомендованы Европейской антиревматической лигой и Американской ассоциацией ревматологов.
Инъекционная терапия ГКС, применяемая в ревматологии уже более 50 лет, считается хорошей альтернативой терапии как пероральными, так и парентеральными нестероидными противовоспалительными препаратами, а также другим способам локального и системного медикаментозного воздействия на воспалительный процесс в суставах. В результате введения суспензии медленно растворимых кристаллов ГКС эффективно подавляется воспаление в синовиальной оболочке, суставной сумке, сухожильных влагалищах и энтезисах [2].
Показанием к локальному введению ГКС служат [2]:
- воспалительные явления в нескольких суставах, суставных сумках, сухожильных влагалищах, энтезиты при исключении их инфекционного генеза;
- артриты отдельных (наиболее болезненных/функционально значимых) суставов у пациентов с полиартритом в ожидании эффекта от системной терапии;
- артриты одного-двух суставов у больных в целом с хорошо контролируемым полиартритом;
- облегчение программ реабилитации (улучшение возможности больного выполнять упражнения лечебной гимнастики);
- противопоказания к другим видам лечения (активная язва желудка, аллергия ко многим препаратам) или их неэффективность.
Противопоказания [1]:
- наличие инфекции в суставе или окружающих тканях; геморрагический синдром;
- тяжелое общее состояние;
- нестабильность сустава;
- асептический некроз в прилежащих эпифизах;
- анатомическая недоступность сустава (резкое сужение щели сустава, его анкилоз);
- механический ритм боли в суставе;
- отсутствие воспалительного процесса;
- отсутствие эффекта (или его кратковременность) от предшествующих двух инъекций.
Характеристика ГКС, применяемых для локальной инъекционной терапии, представлена в табл. 1.
Гиалуроновая кислота ответственна за вязко-эластические свойства синовиальной жидкости, которая выполняет функции лубриканта в суставе. Внутрисуставное введение гиалуроната способствует увеличению синтеза внеклеточных матриксных белков, включая хондроитинсульфат и кератансульфат, а также нормализации состава синовиальной жидкости, ингибированию продукции провоспалительных цитокинов и простагландинов, замедлению катаболических процессов в матриксе хряща. При использовании препаратов гиалуроновой кислоты уменьшается выраженность болевого синдрома и улучшается подвижность сустава, что положительно влияет на качество жизни пациентов [2].
Показаниями для введения гиалуронатов являются:
- остеоартрит;
- механический ритм боли;
- отсутствие признаков синовита;
- рентгенологические первая – третья стадии.
Основные препараты из группы гиалуроновой кислоты представлены в табл. 2.
В лечении остеоартрита более четверти века широко используется комплексный биоактивный препарат Алфлутоп (компания Biotehnos S.A., Румыния) [3]. В его состав входят сульфатированные глюкозаминогликаны, аналогичные матриксу гиалинового хряща: хондроитин-4-сульфат, хондроитин-6-сульфат, дерматансульфат, кератансульфат, низкомолекулярные полипептиды (≤ 50 кДа), свободные аминокислоты и микроэлементы (Na, K, Ca, Mg, Fe, Cu, Zn), имеющие большое значение для обменных процессов и метаболизма соединительной ткани в целом.
Алфлутоп воздействует на внешние рецепторы клеток, такие как СD44, ICAM1, TL-4. Доказано, что препарат способен препятствовать фрагментации внеклеточного матрикса, защищая рецепторы, вовлекаемые в воспалительную реакцию, и блокировать сигнальные пути, активируемые фрагментами матрикса. Как следствие, уменьшается транслокация ядерных провоспалительных факторов.
Именно через рецепторное воздействие Алфлутоп контролирует три компонента синовиального воспаления: клеточную инфильтрацию, высвобождение воспалительных медиаторов и ангиогенез.
Приведенные данные служат обоснованием не только парентерального способа введения Алфлутопа, но и целесообразности локальной доставки препарата в поврежденную область.
При внутрисуставном, периартикулярном или околосухожильном введении Алфлутоп также обладает антигиалуронидазной активностью, что позволяет нормализовать физико-химические свойства синовиальной жидкости в полости сустава, то есть препарат осуществляет функцию своеобразного синовиального протектора [4, 5].
На восьмой Европейской выставке инноваций и изобретений (май 2016 г.) исследователей наградили золотой медалью и дипломом за изучение влияния препарата Алфлутоп на хондроциты на гететическом, клеточном и молекулярном уровнях. В ходе исследования было показано, что под действием препарата Алфлутоп in vitro происходит стимуляция пролиферации и обновления хондроцитов, поддерживается взаимосвязь между клетками и внеклеточным матриксом вследствие модуляции внеклеточного трансформирующего ростового фактора бета в человеческих хондроцитах (CHON-001) – основы для внеклеточных сигналов синтеза структурных протеинов. Эти результаты вместе с результатами о вызванной Алфлутопом in vitro модуляции важных медиаторов воспаления (интерлейкинов 6 и 8, факторов роста эндотелия) служат подтверждением хондровосстановительного эффекта препарата при заболеваниях опорно-двигательного аппарата [6, 7].
Алфлутоп можно вводить внутримышечно, внутрисуставно, паравертебрально, периартикулярно, в болевые точки при фибромиалгии [8].
В зависимости от клинической ситуации схемы введения могут быть следующие:
- в случае вовлечения множества суставов – глубоко внутримышечно по 1 мл ежедневно на протяжении 20 дней;
- в случае вовлечения в процесс крупных суставов – внутрисуставно по 2 мл в каждый пораженный сустав один раз в три дня (шесть введений) с последующим внутримышечным введением по 1 мл ежедневно на протяжении 20 дней;
- при поражении позвоночника – паравертебрально по 0,25 мл в четыре точки (суммарно 1 мл) на уровне двух смежных сегментов дважды в неделю (пять введений) с последующим внутримышечным введением по 1 мл ежедневно в течение 20 дней. Повторение курса лечения целесообразно проводить через три – шесть месяцев [8];
- при полиостеоартрозе и остеохондрозе – глубоко внутримышечно по 1 мл в день (всего 20 инъекций);
- возможно сочетание внутрисуставного и внутримышечного введения. Курс лечения целесообразно повторить через шесть месяцев.
В разных научно-медицинских центрах накоплен значительный положительный опыт применения препарата Алфлутоп при дегенеративных заболеваниях суставов и позвоночника [9–11].
С точки зрения доказательной медицины наиболее интересными являются результаты российского двухлетнего многоцентрового слепого рандомизированного плацебоконтролируемого исследования симптом- и структурно-модифицирующего действия Алфлутопа, проведенного Л.И. Алексеевой и соавт. (2014 г.) [12]. В исследование были включены 90 больных остеоартритом коленного сустава второй и третьей стадий по классификации Kellgren – Lawrence. Пациентов рандомизировали на две группы по 45 человек в каждой: первая получала внутримышечные инъекции Алфлутопа по 1 мл курсами по 20 дней с интервалом шесть месяцев в течение двух лет (всего четыре курса), вторая – инъекции плацебо (изотонический раствор натрия хлорида) по аналогичной схеме. В качестве сопутствующей терапии назначался ибупрофен в дозе 600–1200 мг/сут.
Период наблюдения – два года.
Различия в абсолютной величине снижения интенсивности боли по индексу выраженности остеоартрита университетов Западного Онтарио и МакМастера (Western Ontario McMaster Universities OA Index – WOMAC) между группами оказались достоверными (рис. 1).
Достоверное снижение скованности в группе Алфлутопа наблюдалось к третьему визиту, в группе плацебо значимого снижения не зафиксировано (p
Достоверное улучшение качества жизни отмечено к шестому визиту только в группе Алфлутопа (р = 0,0045). Если в группе Алфлутопа на терапию ответили 73% пациентов, то в группе плацебо – только 40% (р = 0,001).
Терапия Алфлутопом позволила сократить суточную дозу нестероидных противовоспалительных препаратов в 79% случаев и отменить их в 21% случаев. В группе плацебо снижение суточной потребности в нестероидных противовоспалительных препаратах наблюдалось только у 23% больных.
Достоверное замедление сужения суставной щели отмечено у пациентов, получавших Алфлутоп, в отличие от пациентов, получавших плацебо (критерий Вилкоксона, р = 0,0003). При этом у 72% больных второй группы наблюдалось увеличение размеров остеофитов, что значительно больше, чем в первой группе – 27% больных (медиальные и латеральные остеофиты бедренной кости, критерий Вилкоксона, р = 0,0078; медиальные и латеральные остеофиты большеберцовой кости, критерий Вилкоксона, р = 0,0001 и р = 0,0039 соответственно).
Через три месяца лечения Алфлутопом наметилась тенденция к уменьшению уровня маркера деградации хряща С-концевых перекрестных телопептидов коллагена II типа (СТХ-II). Данная тенденция сохранялась до конца исследования, что свидетельствовало об уменьшении деградации суставного хряща. В группе плацебо уровень CТХ-II не изменился (табл. 3).
Исходя из полученных результатов авторы исследования сделали вывод о структурно-модифицирующем эффекте Алфлутопа при остеоартрите коленных суставов.
Препарат замедляет рентгенологическое прогрессирование заболевания (сужение суставной щели и рост остеофитов) и уменьшает деградацию матрикса суставного хряща [13].
Оценка хондропротективного действия Алфлутопа у больных остеоартритом коленного сустава проведена Н.И. Коршуновым и соавт. (2003 г.) [14]. В частности, изучалось действие Алфлутопа на структуры коленного сустава. Период наблюдения составил 12 месяцев.
Пациентам основной группы препарат Алфлутоп вводился сначала внутрь сустава (два раза в неделю, всего шесть инъекций), затем внутримышечно (ежедневно в течение трех недель). Пациенты контрольной группы получали нестероидные противовоспалительные препараты. В течение года было проведено два курса лечения.
Исследование коленных суставов осуществлялось с помощью магнитно-резонансной томографии (МРТ).
Измерение высоты суставного хряща проводилось в трех точках: в области передней (первая точка) и задней (вторая точка) поверхности головки бедренной кости, а также в точке наибольшего соприкосновения бедренной и большеберцовой костей (третья точка) коленного сустава. При этом в первой и второй точках определялась высота суставного хряща бедренной кости, а в третьей – суммарная толщина хряща бедренной и большеберцовой костей. При визуальной оценке МРТ независимым экспертом в основной группе улучшение наблюдалось у 10 (40%) больных, ухудшение – у 3 (12%), отсутствие изменений – у 12 (48%) больных. В контрольной группе улучшение было зарегистрировано у 4 (17%) больных, ухудшение – у 7 (29%), отсутствие изменений – у 13 (54%) больных.
МРТ коленного сустава у пациента с остеоартритом до лечения Алфлутопом и после представлена на рис. 3.
Согласно результатам трехлетнего проспективного наблюдения, проведенного В.Н. Дроздовым и Е.В. Коломиец (2005 г.), включение Алфлутопа в комплексную терапию больных гонартрозом второй и третьей стадии позволяет значительно сократить или полностью отказаться от приема нестероидных противовоспалительных препаратов, что снижает или исключает риск их повреждающего воздействия на желудочно-кишечный тракт [15].
Данные, полученные И.Г. Салиховым [16] и Н.А. Хитровым [17], подтверждают эффективность параартикулярного введения Алфлутопа у больных гонартрозом с признаками поражения сухожильно-связочного аппарата, а также с энтезопатиями надостной и/или подлопаточной мышц. Курсовое введение препарата в болевые точки, соответствующие энтезисам пораженных мышц (2 мл Алфлутопа с 15 мл 0,25%-ного раствора новокаина два раза в неделю, всего пять инъекций), приводило к уменьшению болей в плечевом суставе по Визуальной аналоговой шкале, увеличению объема движений, снижению дозы принимаемых нестероидных противовоспалительных препаратов на 30–70%.
Алфлутоп также продемонстрировал эффективность у неврологических больных. В двойном слепом плацебоконтролируемом исследовании О.С. Левина и соавт. препарат назначался при хронической вертеброгенной люмбоишиалгии. Наиболее эффективной терапия Алфлутопом оказалась у пациентов молодого и среднего возраста с относительно короткой продолжительностью заболевания и текущего обострения, при поражении фасеточных суставов [8].
В исследовании сравнивалась эффективность внутримышечного введения Алфлутопа (20 инъекций по 1 мл) у 32 больных и паравертебрального (по 0,25 мл в четыре точки (суммарно 1 мл) на уровне двух смежных сегментов два раза в неделю, всего пять инъекций) у 22 больных. Состояние пациентов оценивалось через один, три и шесть месяцев.
Исходно у всех участников исследования диагностировали некорешковую/корешковую вертеброгенную люмбоишиалгию, умеренный или выраженный болевой синдром, хроническое или рецидивирующее течение с длительностью обострения не менее месяца.
Уже через месяц терапии Алфлутопом отмечено достоверно отличающееся от плацебо уменьшение и вертеброгенного синдрома, и боли. При этом более выраженный эффект лечения отмечен в группе больных, которым препарат вводили паравертебрально. Через три месяца от начала применения Алфлутопа степень нарастания терапевтического эффекта также была выше у тех, кому препарат вводился паравертебрально.
Авторы исследования рекомендовали при обострении вертебральной люмбоишиалгии начинать курс лечения с паравертебральных инъекций, затем переходить на внутримышечные (20 инъекций). Это позволяет достоверно улучшить функциональное состояние больных и купировать болевой синдром на длительный срок.
При синдроме хронической боли в нижней части спины ее нивелирование после первого курса Алфлутопа отметили 7,1% больных, после второго – 35,7%. Таких результатов не зафиксировано у пациентов контрольной группы. В основной группе установлено также достоверное ступенчатое (p = 0,001) снижение показателей пробы Томайера: через три месяца после завершения лечения Алфлутопом они уменьшились в 3,6 раза. За период лечения у пациентов этой группы отмечено увеличение объема статической и динамической нагрузки на позвоночник (по индексу хронической нетрудоспособности Ваделя) в 2–2,5 раза. По его окончании 42,9% пациентов основной группы и только 5,6% пациентов контрольной группы прекратили прием нестероидных противовоспалительных препаратов [15].
Приведенные результаты научных исследований свидетельствуют о том, что препарат Алфлутоп обладает хондропротективным, противовоспалительным, трофическим действием, доказанным быстро развивающимся клиническим эффектом, продолжительным периодом последействия (четыре – шесть месяцев), высоким профилем безопасности и может быть рекомендован для широкого применения в ревматологической, неврологической, терапевтической, травматологической и ортопедической практике.
Сказанное выше позволяет сделать следующий вывод: на сегодняшний день внутрисуставная инъекционная терапия заболеваний опорно-двигательного аппарата является эффективным методом лечения. Результативность и переносимость пациентами данного вида лечения зависят от знания анатомо-топографических особенностей, оценки состояния пораженного сустава и точного выполнения техники внутрисуставных инъекций.
Источник
