Эпидуральная анестезия операции на позвоночнике
Анестезия при операции на поясничном отделе позвоночника. Послеоперационный уход
• Из-за положения на операционном столе и длительности операций (особенно при обширных процедурах) при большинстве операций применяется общая анестезия.
• Субарахноидальиая анестезия используется при одноуровневых операциях на поясничном отделе.
• Хирурги могут попросить снизить артериальное давление с целью уменьшения кровопотери и улучшения визуализации. Поскольку эта дилемма чаще возникает при корректикующей, многоуровневой спинальной хирургии или вертебрэктомии при опухолях, следует помнить о потенциальном риске спинальной ишемии. У пожилых пациентам с сопутствующими заболеваниями шинельная перфузия может быть менее полноценной, поэтому они особо подвержены рискам.
• Венозный доступ крупного диаметра должен быть доступен и при положении пациента на животе.
• Интраартериальный мониторинг АД необходим при обширных процедурах и в случае серьезных заболеваний сердца. При одноуровневой спинальной операции (например, дискэктомии) в целом здоровому пациенту артериальный катетер не требуется.
• Кровопотсря обычно в пределах 50-500 мл, но может быть выше при одновременной многоуровневой декомпрессии. Кровотечение из эпидуральпых вен может быть внезапным и профузным, при этом рекомендуется проводить аутогемотрансфузию. Операция длится от 45 минут при одноуровневой дискэктомии до 2-4 часов при обширной ламинэктомии.
Положение на операционном столе при операции на поясничном отделе позвоночника:
• Обычно при операциях на поясничном отделе из заднего доступа пациент лежит на животе. Однако возможно выполнение в положении на боку (например, дискэктомия при беременности).
• Обычно пациент лежит на валиках или раме Вилсона, но используется и опора на колени и грудную клетку.
• Голова обычно лежит на подковообразном подголовнике или подходящей опоре.
• Положение на животе при спинальных операциях связано с риском воздушной змболии.
• Необходимо избегать давления на брюшную стенку, подвздошные гребни, подмышечные области и лицо (особенно глаза).
Послеоперационный уход при операции на поясничном отделе позвоночника:
• Интенсивность послеоперационного болевого синдрома зависит от объема удаления кости.
• Микродискэктомии может выполняться при минимальном удалении костной ткани, и некоторые пациенты могут быть выписаны домой в день операции.
• При лечении крупных или центральных протрузий диска или ламинэктомии требуется более широкий доступ, что требует назначения опиоидов в течение нескольких дней после операции, и часто используется контролируемая пациентом анальгезия.
• Интра- и послеоперационная анальгезия предусматривает комбинацию сильных опиоидов и НПВС или парацетамола.
Советы анестезиологам при операции на поясничном отделе позвоночника:
• Обширные операции (многоуровневых или по поводу опухолей) нередко сопровождаются значительной кровопотерей. Может использоваться ауто-гемотрасфузия.
• Перед началом анестезии уточните у хирурга требуемое положение на столе и вид поддержки при положении пациента па животе.
• Хотя подкожная местная анестезия уменьшает боль при разрезе, анальгезия более глубоких структур недостаточная.
• Длительные операции в положении на животе могут привести к послеоперационной потере зрения.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Предоперационная оценка при опухолях и сосудистых мальформациях спинного мозга. Критерии анестезиолога”
Оглавление темы “Анестезия в спинальной хирургии”:
- Анестезия при передней шейной дискэктомии. Послеоперационный уход
- Анестезия при верхней шейной декомпрессии задней черепной ямки (ВШДЗЧЯ) – аномалии Киари. Послеоперационный уход
- Осмотр перед операцией на поясничном отделе позвоночника. Критерии анестезиолога
- Анестезия при операции на поясничном отделе позвоночника. Послеоперационный уход
- Предоперационная оценка при опухолях и сосудистых мальформациях спинного мозга. Критерии анестезиолога
- Анестезия при опухолях и сосудистых мальформациях спинного мозга. Послеоперационный уход
- Предоперационная оценка при спинальной травме. Критерии анестезиолога
- Анестезия при спинальной травме. Послеоперационный уход и прогноз
- Анестезия при имплантации баклофеновой помпы. Предоперационная оценка
- Анестезия при дефектах нервной трубки. Ведение пациентов со спинальной мальформацией
Источник
СПИНАЛЬНАЯ И ЭПИДУРАЛЬНАЯ АНЕСТЕЗИЯ: ПРЕИМУЩЕСТВА
В этой статье мы подробнее остановимся на отдельных видах регионарной анестезии, которые являются наиболее популярными и востребованными на сегодняшний день.
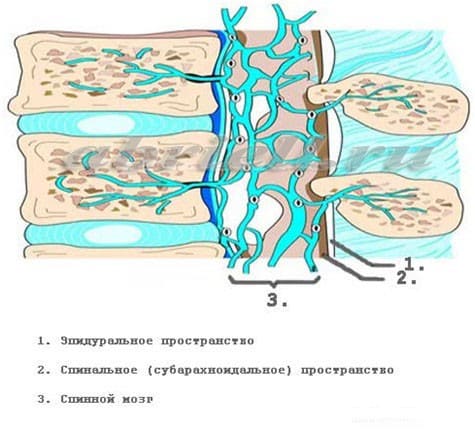
В этой части Вам встретятся некоторые медицинские термины, без которых, к сожалению, невозможно обойтись. Для начала хотим показать Вам некоторые рисунки, на которых отражено строение нашего позвоночника. Обратите внимание на два сектора, субарахноидальное пространство и эпидуральное пространство, и как они располагаются по отношению к спинному мозгу:
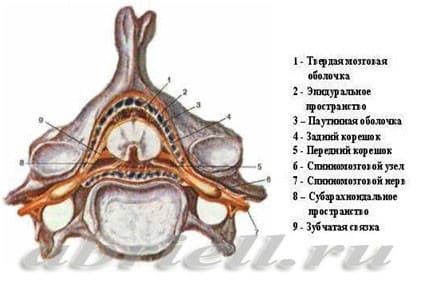 Рисунок 1 и 2. Спинной мозг и его оболочки, показанные на поперечном разрезе позвоночника
Рисунок 1 и 2. Спинной мозг и его оболочки, показанные на поперечном разрезе позвоночника
Спинномозговой канал имеет три соединительнотканные оболочки, защищающие спинной мозг: твердую мозговую оболочку, паутинную (арахноидальную) оболочку и мягкую мозговую оболочку. Непосредственно спинной мозг и его корешки укрывает хорошо васкуляризированная мягкая мозговая оболочка, а субарахноидальное пространство отграничено двумя прилегающими друг к другу оболочками – паутинной и твердой мозговой.
 Рисунок 3. Спинной мозг и его оболочки в другой плоскости.
Рисунок 3. Спинной мозг и его оболочки в другой плоскости.
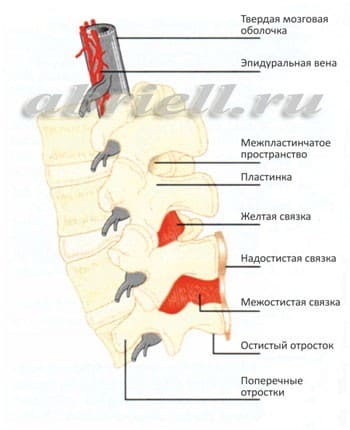
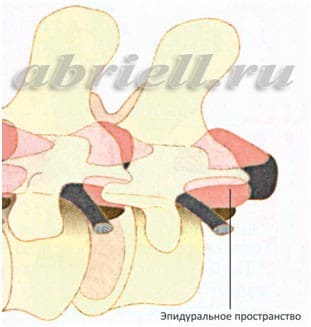
Рисунок 4 и 5. Оболочки спинного мозга в объёмном изображении. На рисунке 4 эпидуральное пространство находится до твёрдой мозговой оболочки (серый цилиндр), а спинной мозг лежит внутри этого цилиндра.
СПИНАЛЬНАЯ АНЕСТЕЗИЯ
Спинальная анестезия – является одним из наиболее популярных на сегодняшний день методов анестезии. Для спинальной анестезии применяются препараты, хорошо знакомые вам по стоматологической практике: лидокаин, маркаин. При этом виде обезболивания происходит блокада всех видов чувствительности (в первую очередь болевые сигналы), которая вызывается введением анестетика (препарат, блокирующий чувствительность) в ликвор, заполняющий субарахноидальное пространство спинномозгового канала. Во время манипуляции местный анестетик вводится в область, располагающуюся близко к спинному мозгу. Однако, спинной мозг не затрагивается, так как используется очень тонкая игла, которая вводится в субарахноидальное пространство ниже его окончания, то есть только на поясничном уровне и ниже второго поясничного позвонка. Показательны следующие рисунки:
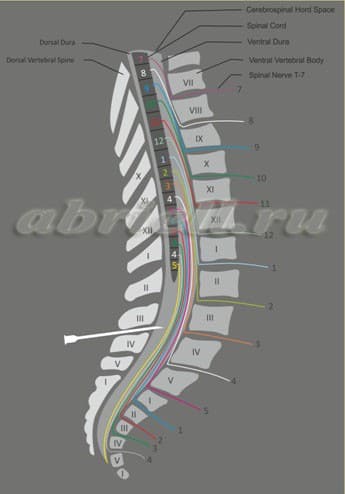 Рисунок 6. В субарахноидальное пространство введён местный анестетик, он распространился вверх и блокирует нервы, свободно «плавающие» в ликворе.
Рисунок 6. В субарахноидальное пространство введён местный анестетик, он распространился вверх и блокирует нервы, свободно «плавающие» в ликворе.
В зависимости от вида вводимого местного анестетика, при спинальной анестезии можно добиться разного по распространённости и продолжительности обезболивания. Мы используем препараты, вызывающие те же эффекты, что и эпидуральная анестезия, но на уровне от нижних отделов живота (ниже уровня пупка) до стоп. Поэтому, при данном виде обезболивания можно выполнять следующие операции:
– липофилинг голеней;
– липосакция в области ног;
– липосакция талии;
– подтяжка ягодиц;
– эндопретезирование ягодиц и др.
Преимущества спинальной анестезии:
(а) затрачивается меньше времени на проведение;
(б) намного быстрее развивается сегментарная блокада;
(в) по качеству обезболивания блокада лучше.
ЭПИДУРАЛЬНАЯ АНЕСТЕЗИЯ
Эпидуральная анестезия – так же является одним из самых популярных методов анестезии. Для эпидуральной анестезии применяются препараты: лидокаин, маркаин, наропин. Анестетик вводят в пространство над твердой мозговой оболочкой спинного мозга. При этом блокируются все виды чувствительности от отделов, которые расположены в зоне действия анестетика. Чаще всего, при эпидуральной анестезии, в область прокола вводят сначала иглу, а по ней мягкую гибкую трубочку – катетер, по которому в случае необходимости можно добавлять лекарство, иглу же вынимают.
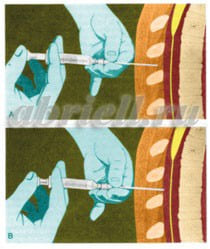
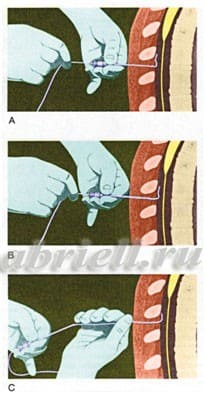 Рисунок 7. Через иглу вводится специальный катетер.
Рисунок 7. Через иглу вводится специальный катетер.
Процедура установки эпидурального катетера выполняется в стерильных условиях под местным обезболиванием, практически безболезненна, могут быть только неприятные ощущения при продвижении иглы или катетера.
Учитывая анатомические особенности расположения эпидурального пространства (отделено от спинного мозга несколькими мозговыми оболочками – твердой, паутинной и мягкой), введение катетера может выполняться, как на грудном, так на поясничном уровне. Структуры спинного мозга при этом абсолютно не затрагиваются.
Поэтому, для пластических операций эпидуральная анестезия может выполняться на верхнем уровне (например, для выполнения абдоминопластики) и заканчивая нижним уровнем (липофиллинг голеней). В послеоперационном периоде может продолжаться постоянное обезболивание многочасовым введением препарата специальным дозирующим устройством, при этом пациент активен, ведёт удобный для него образ жизни до выписки из клиники.
Преимущества эпидуральной анестезии:
- значительно меньше риск развития головных болей;
- способность удлинить блок, вводя дополнительные дозы препарата через установленный в эпидуральное пространство катетер во время операции;
- есть возможность использовать катетер после операции для дальнейшего обезболивания в палате.
Противопоказания для спинальной и эпидуральной анестезий общие:
- Нарушение свёртывающей системы крови
- Инфекция в месте пункции
Возможные осложнения:
- Боль в спине и пояснице. По сравнению со спинальной анестезией, боль в спине после эпидуральной анестезии возникает чаще и продолжается дольше. Интенсивность болей не значительная, но в одном из исследований упоминается, что боль в спине становится наиболее частой причиной отказа пациентов от эпидуральной анестезии в будущем. Причина этого осложнения чётко не выяснена, хотя в качестве объяснения выдвигаются следующие предположения: травма окружающих тканей иглой, растяжение связочного аппарата позвоночника. В течение нескольких дней боли проходят самостоятельно, можно 3-5 дней принимать найз, индометацин, диклофенак, посоветовавшись предварительно с врачом.
- Головные боли. Чаще возникает после спинальной анестезии. Характеризуются умеренными проявлениями или вообще их отсутствием в положении на спине и значительным усилением в лобно-затылочной области при подъёме головы. У большинства пациентов головные боли проходят самостоятельно от нескольких дней до недели. Лечение же включает постельный режим, обильное питьё, по необходимости обезболивание, дополнительное введение растворов в вену. Установлено положительное влияние от кофеина.
- Неврологические повреждения. Возникают редко и связаны с введением местных анестетиков высокой концентрации, которые не применяются в нашей клинике.
- Эпидуральная гематома. Очень редкое осложнение, в основном связанное с патологией свёртывающей системы крови или приёмом пациентами некоторых препаратов, которые увеличивают кровоточивость.
СПИНАЛЬНАЯ И ЭПИДУРАЛЬНАЯ АНЕСТЕЗИЯ: вместо заключения
Абсолютных показаний для спинальной и эпидуральной анестезии не существует, то есть, нет таких ситуаций, когда могут применяться только эти виды анестезии и ничего более. Но есть положения (например, предпочтения пациента, общее состояние его здоровья, место операции), при которых спинальная и эпидуральная анестезия становятся методами выбора (то есть, желательно проводить именно их). В эстетической хирургии, эти методы являются методами выбора, учитывая цели анестезии, о которых уже упоминалось ранее:
- Прекрасное обезболивание во время операции;
- Используется мало препаратов для наркоза;
- Меньшее воздействие анестезии на функцию различных систем органов;
- Значимо меньше кровопотеря;
- Меньше тромбоэмболических осложнений;
- Ранняя активизация;
- Снижение частоты малых осложнений анестезии: тошнота, рвота, сонливость;
- Возможность проводить более качественное обезболивание после операции.
Показательными примерами являются операции на ягодицах, когда пациентка во время операции лежит на животе. Спрашивается, зачем создавать неудобства, которые непременно придётся испытывать всем членам бригады и самой пациентке, если проводить общую анестезию с установкой трубки в дыхательные пути, когда есть прекрасным метод спинальной анестезии?
Данные методики анестезии могут улучшить результаты эстетических операций, так как способствуют снижению кровопотери во время операции, уменьшению частоты тромбозов, что наиболее актуально при липосакции, абдоминоплатике, особенно когда эти операции выполняются в комбинации.
На сегодняшний день, с совершенствованием дизайна игл, структуры катетеров, материалов из которых изготовляются эти приспособления, обширной техникой слежения за состоянием пациента в операционной, методика спинальной и эпидуральной анестезии стала практически безопасной.
ПОДГОТОВКА К ОПЕРАЦИИ: ПОДГОТОВКА К НАРКОЗУ (ОБЩЕЙ АНЕСТЕЗИИ)
В настоящей памятке по подготовке к операции подробно описано как готовится к общему наркозу, какие соблюдать правила и условия.
ПОДГОТОВКА К ОПЕРАЦИИ: АНКЕТА АНЕСТЕЗИОЛОГА
Такой опросник Вы будете заполнять вместе с анестезиологом при подготовке к операции либо на предварительной консультации или непосредственно перед операцией. Здесь для Вашего спокойствия перечислены основные важные вопросы, на которые необходимо четко и верно отвечать для определния наилучшего анестезиологического пособия хирургической операции.
 ПОДГОТОВКА К АНЕСТЕЗИИ
ПОДГОТОВКА К АНЕСТЕЗИИ
Еще раз остановимся на том как подготовится к наркозу, какие есть важные особенности и рекомендации.
ПОДГОТОВКА К ОПЕРАЦИИ: СПИСОК АНАЛИЗОВ ДЛЯ ОПЕРАЦИИ
В этой памятке для пациентов перечислены все основные лабораторные исследования и обследования у врачей специалистов, которые необходимо выполнить при подготовке к операции, как для местной анестезии так и для общего наркоза.
АНАЛИЗЫ ДЛЯ ОПЕРАЦИИ В КЛИНИКЕ “АБРИЕЛЛЬ”
Для Вашего удобства при подготовке к операции Вы можете пройти все необходимые лабораторные исследования в клинике “Абриелль”. Вы можете сделать это в любое удобное для Вас по предварительной записи с 9.00 до 21.00 ежедневно. Вся процедура займет у Вас не более 15- 20 минут. Результаты исследований будут готовы в течение 1 – 3 дней, их сразу оценивает врач-анестезиолог. Если понадобится дополнительные обследования с Вами свяжутся и запишут на консультацию.
Источник
А.В. Соленкова, А. Ю. Лубнин, О. Г. Арестов, И.Н. Шевелев
НИИ нейрохирургии им.Н.Н.Бурденко РАМН, Москва
Введение. В настоящее время эпидуральная анестезия (ЭА) занимает одно из ведущих мест в структуре анестезиологического обеспечения в самых различных областях хирургии: абдоминальной, торакальной, кардиохирургии, травматологии и ортопедии, оперативной урологии и гинекологии, а также в акушерстве. Однако к применению ЭА при операциях на позвоночнике и спинном мозге отношение неоднозначное. Так, в ряде руководств по анестезиологии и регионарной анестезии патология позвоночника и спинного мозга рассматривается как относительное противопоказание к проведению ЭА. Существует мнение, что патологические изменения позвоночника и элементов позвоночного канала определяют противопоказания к использованию ЭА, так как затрудняют пункцию и идентификацию эпидурального пространства, влияют на распространение анестетика по эпидуральному пространству, создают основу для увеличения числа осложнений и случаев неэффективной блокады спинномозговых корешков. В то же время, в литературе встречаются единичные сообщения об успешном применении данного вида анестезии у больных со спинальной патологией.
Целью настоящего исследования явилась комплексная оценка эффективности и безопасности ЭА при оперативных вмешательствах на позвоночнике и спинном мозге, когда хирургическая травма наносится в непосредственной близости от центральных структур, проводящих болевую импульсацию, и долгое время находящихся в изменённом состоянии
Материал и методы исследования. В основу работы положены данные клинического исследования 122 больных с патологией позвоночника и спинного мозга на поясничном и крестцовом уровнях. Возраст больных колебался от 26 до 78 лет (средний 43,9 ± 8,8 лет). У 92,7 % больных физический статус оценивался как I-II класс по ASA и только у 7,3 % больных он соответствовал III классу. Предоперационная неврологическая симптоматика включала в себя выраженный болевой синдром, как в спине, так и в нижних конечностях, нарушения чувствительности в нижних конечностях и преходящие нарушения функции тазовых органов. Характеристика больных приведена в таблице 1.
Таблица 1. Распределение больных по основной нейрохирургической патологии,
а также избранному методу анестезии.
| Нейрохирургическая патология | Эпидуральная анестезия | Общая анестезия (ОА) |
| Грыжи межпозвонковых дисков | 76 | 36 |
| Стенозы позвоночного канала | 3 | |
| Опухоли позвоночника и спинного мозга: Экстрадуральные | 3 | 4 |
| Итого: (n=122) | 82 | 40 |
Основной контингент составили больные с грыжами межпозвонковых дисков на пояснично-крестцовом уровне.
В соответствии с целью исследования сравнительная оценка показателей гемодинамики и функции дыхания была проведена у 80 больных, оперированных по поводу патологии позвоночника и спинного мозга на поясничном-крестцовом уровне. В зависимости от вида использованной анестезии (ЭА или ОА) больные были разделены на две группы, сопоставимые по антропометрическим характеристикам. В исследуемой группе все больные были оперированы в условиях ЭА местными анестетиками (МА) в сочетании с в/в седацией комбинацией препаратов (диприван 3,8 + 0,3 мг/кг/ч + реланиум 10-15 мг, диприван 3,8 + 0,3 мг/кг/ч + дормикум 5-10 мг) с сохраненным самостоятельным дыханием и ингаляцией О 2 через маску. В контрольной группе использовалась комбинированная ОА (НЛА) с миорелаксантами и интубацией трахеи (реланиум 10-15 мг, диприван: индукционная доза 1,95 ± 0,5 мг/кг, поддерживающая 5,3 + 0,4 мг/кг/ч, фентанил 2,0 + 0,5 мкг/кг/ч). В процессе подготовки к операции всем больным назначалась премедикация, включающая в себя феназепам в дозе 1,0-1,5 мг/кг вечером накануне операции и утром в день операции.
ЭА выполняли в условиях операционной при полноценном мониторинге. В асептических условиях под местной анестезией 0,25% раствором новокаина в положении больного на боку выполняли пункцию и катетеризацию эпидурального пространства на 1-2 межпозвонковых промежутка выше верхнего края предполагаемого разреза, с использованием стандартной техники и одноразовых наборов «Perifix» (B.Braun, Германия). Катетер проводили краниально на 1,5-2,0 см. В качестве МА использовали 0,25-0,5% раствор бупивакаина (маркаина) фирмы Astra Zeneca , вводимая доза составляла 50-125 мг, а объём раствора 15-25 мл. Основную дозу анестетика вводили через катетер в положении больного на спине. Сенсорный и моторный блок развивались через 20-30 минут. Затем больного укладывали в положение необходимое для проведения операции (на левом или правом боку с приведенными к животу коленями). При необходимости вводили повторную дозу МА – 25 мг, как во время операции, так и в первые сутки послеоперационного периода. В группе больных, оперируемых под ОА, в послеоперационном периоде использовали нестероидные противовоспалительные препараты.
В ходе анестезии и операции мониторировали ЭКГ в 3-х отведениях, АД (систолическое, диастолическое и среднее), пульсовую оксиметрию и капнографию при помощи 8 – канального монитора фирмы Hewlet-Packard США. У больных исследуемой группы контроль за адекватностью самостоятельного дыхания осуществляли с помощью side – stream блока того же монитора, а также периодическим исследованием параметров КОС и газового состава капиллярной крови (Blood Gas analyser 178 фирмы CIBA-Corning США). Были выделены следующие этапы, на которых регистрировались параметры гемодинамики и внешнего дыхания: 1 – за 30 минут до операции (до проведения ЭА), 2 – после выполнения блокады или индукции анестезии, перед кожным разрезом, 3 – в наиболее травматичный момент операции (ламинэктомия или скелетирование позвонков), 4 – в конце операции, 5 – через 2 часа после операции.
Эффективность обезболивания в послеоперационном периоде оценивали по 10-бальной визуально-аналоговой шкале (ВАШ). Все полученные числовые значения были подвергнуты статистическому анализу с помощью пакета программ “graph”.
Результаты и их обсуждение. В ходе исследования мы не выявили нарушений функции дыхания, как в группе с ИВЛ, так и в группе с самостоятельным дыханием. У последних больных на фоне глубокой седации отмечалось незначительное снижение частоты дыхания и повышение РаСО 2 максимально до 46 мм.рт.cт., что позволило связать наблюдаемые сдвиги с эффектом дипривана.
Гемодинамические показатели. Средние величины АД и ЧСС в начале исследования были близкими в контрольной и исследуемых группах (табл.2).
Таблица 2. Динамика показателей гемодинамики и функции внешнего дыхания
на этапах исследования
| Этапы | Группы | Адс мм рт ст | Адд мм рт ст | Адср мм рт ст | ЧСС в` | Et CO2 | ЧД |
| I | 1-я (n – 9) | 142,2 ± 5,1 | 82,2 ± 6,2 | 104,1 ± 5, 1 | 84,7 ± 2,5 | 15,7 ± 2,5 | |
| I | 2-я (n – 9) | 138 ± 5,5 | 78,7 ± 2,1 | 100,2 ± 2,4 | 82,4 ± 2,7 | 16,1 ± 2,2 | |
| II | 1-я n – 9) | 125,9 ± 4,4 | 63,7 ± 3,1 | 91,7 ± 2,9 | 74,7 ± 3,3 | 38,7 ± 2,5 | 11,5 ± 1,9 |
| II | 2-я n – 9) | 106,7 ± 2,9* | 55,8 ± 2,7 | 77,0 ± 2,6* | 65,7 ± 2,3 | 30,2 ± 1,0 | 12,0,7 ± 15 |
| III | 1-я (n – 9) | 102,1 ± 3,8 | 54,5 ± 2,3 | 76,2 ± 2,8 | 73,6 ± 6,1 | 33,7 ± 1,2 | 10,9 ± 2,1 |
| III | 2-я (n – 9) | 135,2 ± 6,9* | 66,0 ± 6,5 | 93,6 ± 6,4* | 78,0 ± 6,0 | 29,7 ± 1,0 | 11,3 ± 1,4 |
| IV | 1-я (n – 9) | 114,3 ± 2,4 | 57,2 ± 1,9 | 81,6 ± 3,1 | 74,1 ± 2,5 | 31,7 ± 1,5 | 12,7 ± 1,5 |
| IV | 2-я (n – 9) | 124,2 ± 4,7 | 63,4 ± 4,1 | 89,0 ± 5,3 | 85,7 ± 1,9 | 30,0 ± 1,5 | 10,7 ± 1,0 |
| V | 1-я (n – 9) | 128,0 ± 3,2 | 71,1 ± 2,5 | 93,3 ± 3,7 | 69,1 ± 1,3 | 15,3 ± 1,5 | |
| V | 2-я (n – 9) | 130,4 ± 4,0 | 68,9 ± 3,5 | 92,8 ± 3,4 | 78,6 ± 2,4 | 14,2 ± 2,4 |
К моменту начала хирургических манипуляций (2 этап исследования) в обеих группах было отмечено снижение значений систолического, диастолического и среднего АД, а также ЧСС по сравнению с 1 этапом, что, по-видимому, объясняется снятием психоэмоционального напряжения и устранением дооперационного болевого синдрома при переходе больных в состояние общей анестезии (контрольная группа) или глубокой седации, достигаемой с помощью в/в инфузии дипривана (исследуемая группа). Интересно, что наиболее выраженным это снижение было не в исследуемой, а в контрольной группе больных. Известно, что снижение АД является характерным феноменом для клиники ЭА и даже служит косвенным показателем ее эффективности. Диприван при введении в индукционных дозах также обладает гипотензивным эффектом, сопоставимым с таковым у барбитуратов. Поэтому, мы вправе были ожидать развития выраженной артериальной гипотензии на 2-м этапе именно в исследуемой группе, вследствие аддитивного эффекта дипривана при сочетании с ЭА. Однако, полученные нами данные свидетельствуют о том, что комбинация препаратов НЛА с диприваном обладает более выраженным гипотензивным эффектом, чем комбинация ЭА + диприван на этапе индукции анестезии (перед кожным разрезом). Достаточно выраженное снижение ЧСС в контрольной группе также, по-видимому, отражает эффект наркотических анальгетиков.
Наибольший интерес представляла динамика АД и ЧСС на 3-м этапе исследования, который характеризовался высокой травматичностью (смещение дурального мешка и тракция спинномозгового корешка). Были получены статистически достоверные различия (р<0,05) между группами, причем в исследуемой группе больных отмечено дальнейшее снижение величин АД сист , АД диаст . и АД сред при неизменных значениях ЧСС, тогда как в контрольной группе величины АД сист и АД сред повысились по сравнению с предыдущим этапом. Увеличилась и ЧСС, хотя отличие статистически не значимо. Такая реакция гемодинамических параметров на наш взгляд свидетельствует о недостаточной защите организма оперируемого больного от ноцицептивной стимуляции на этом этапе в условиях ОА. Cледует подчеркнуть, что на фоне внутривенного введения дипривана снижение АД у больных, оперируемых в условиях ЭА, не превышало 26%-28% от исходных величин, хорошо контролировалось изменением скорости вводимого препарата, инфузионной нагрузкой, либо использованием эфедрина в дозе 5-10 мг внутривенно. Данную коррекцию осуществляли при снижении АД сист не более чем на 25% от исходного показателя и АД сред для нормотоников ниже 75 мм.рт.ст. Следует подчеркнуть, что даже глубокая гипотензия достаточно быстро купировалась перечисленными выше приемами и не создавала особых проблем для анестезиолога.
Этап окончания операции характеризовался сближением показателей гемодинамики в обеих группах, по сравнению с предыдущим этапом – незначительным повышением АД в исследуемой и наоборот снижением в контрольной группе. Через 2 часа после операции значения всех гемодинамических показателей в обеих группах были близкими между собой по величине.
Эффективность послеоперационного обезболивания. Обеспечение адекватного послеоперационного обезболивания дает возможность более быстрого функционального восстановления организма больного после операции, способствует ранней активизации и соответственно сокращает сроки пребывания в стационаре. Результаты субъективной оценки пациентами болевых ощущений сразу после операции, в ближайшие 2 часа послеоперационного периода, в 1 сутки после операции и на 2 и 3 сутки после операции представлены на рисунке 1.
| Рис.1. Субъективная оценка эффективности обезболивания в послеоперационном периоде (М ± м) 0-3 балла – эффективная аналгезия >4 баллов – неэффективная аналгезия |
Были отмечены статистически достоверные различия между группами на следующих этапах: через 2 часа после операции, в 1-е и 2-е сутки после неё. Пра ктически отсутствовали болевые ощущения у пациентов в группе ЭА через 2 часа после операции (1,9 ± 0,43 балла). Достаточно интенсивный болевой синдром отмечался через 2 часа после операции в группе ОА (5,6 ± 1,4 балла). В течение 1-2-х суток после операции больные в группе с ЭА отмечали незначительный дискомфорт в области операционной раны при изменении положения тела (2,6 ± 0,56 балла и 2,5 ± 0,7 балла).
Пациенты группы ОА ощущали боль средней интенсивности в покое и при изменении положения тела (5,2 ± 1,08 балла и 5,1 ± 1,2), которая лишь кратковременно купировалась аналгетиками. При опросе больных на 3-и сутки после операции не было выявлено статистически значимых различий в двух группах, клинически этот этап характеризовался практически отсутствием болей в области операционной раны.
Ранние послеоперационные осложнения. При анализе послеоперационных осложнений, связанных непосредственно с методикой анестезии были получены следующие результаты (табл.3). Для больных, оперированных в условиях ОА, была характерна высокая частота тошноты и рвоты (22,5%) в раннем послеоперационном периоде.
Таблица 3. Ранние послеоперационные осложнения
| Осложнения | Эпидуральная анестезия (n=40) | Общая анестезия (n=40) |
| Головная боль | 1 (2,5%) | |
| Тошнота | 1(2,5%) | 7 (17,5%) |
| Рвота | 2 (5%) | |
| Задержка мочи < 2 дней | 2 (5%) | 5 (12,5%) |
| Задержка мочи > 2 дней | 1(2,5%) | |
| Сенсорные изменения (дизестезии) | 1 (2,5%) | |
| Инфекционные осложнения | ||
| Послеоперационный неврит | 3 (7,5%) | 3 (7,5%) |
| Ангина и фарингит | 2 (5%) | |
| Постинтубационная травма мягкого неба | 1 (2,5%) |
Важно отметить, что временная задержка мочи чаще встречалась при использовании ОА – у 15% больных, по сравнению с ЭА – 5% больных. Наши результаты относительно частоты послеоперационной задержки мочи совпадают с результатами Greenberg и соавт. (1988), которые сообщили о снижении числа случаев острой послеоперационной задержки мочи у больных, оперируемых в условиях ЭА, по сравнению с ОА. Silver D ..и соавт. (1976) отметили, что частота послеоперационной задержки мочи при ОА составляет 7%, а при спинальной анестезии всего 2,76%.
С позиций операционного стресса этот момент может объясняться достаточно выраженной активацией симпатической нервной системы, выбросом гормонов стресса, которые воздействуют на различные органы – мишени (в том числе почки), спазмируют сосуды и снижают почечный кровоток, а также способствуют выбросу кортизола из коры надпочечников. ЭА, как указывает Bonica J . (1957), устраняя рефлекторную почечную вазоконстрикцию, предупреждает развитие олигурии. Определенную роль в возникновении задержки мочи также играет степень остаточной седации, которая более выражена при использовании ОА. Существует также точка зрения, что ЭА устраняет дисфункцию детрузора и сфинктера мочевого пузыря, возникающую при компрессии структур позвоночного канала.
Из осложнений, связанных непосредственно с эпидуральной анестезией, необходимо отметить 2 случая возникновения после операции гипостезии: 1-й – в области дерматома L 2 слева, соответствующего уровню пункции эпидурального пространства, 2-й в проекции веточек кожного нерва, вследствие длительного позиционного сдавления. Гипостезия регрессировала самостоятельно в течении 3 суток после операции. Разграничить сенсорные и моторные нарушения, которые могут возникнуть как в результате выполнения эпидуральной блокады, так и в ходе самой операции (грубая тракция или повреждение спинномозговых нервов) можно учитывая особенности сегментарной иннервации спинного мозга. Так нарушения иннервации в зоне операции (чаще уровень L 4- L 5- S 1) дают изменения именно в соответствующих дерматомах.
В заключении хотелось особо отметить некоторые особенности ЭА при патологических изменениях структур позвоночного канала, которые обнаруживаются при удалении грыж поясничных межпозвонковых дисков. Так недостаточная анальгезия кожи в зоне операции была отмечена у 5 больных. Клинически это проявилось двигательной и вегетативной реакцией, но введение 0,025-0,05 мг фентанила и углубление медикаментозной седации позволило выполнить запланированный объём операции. На этапе удаления грыжи межпозвонкового диска при смещении дурального мешка и тракции спинномозгового корешка у 7 больных возникали спонтанные сокращения мышц соответствующей ноги. Но отсутствие у них вегетативной реакции на боль позволяло считать наблюдаемые мышечные сокращения проявлением прямого раздражения двигательных нервов.
Недостаточная анальгезия зоны операции, потребовавшая перехода на общее обезболивание, была отмечена у 3 больных. У 2 из них на операции был обнаружен грубый рубцово-спаечный процесс, и в одном случае имели место дефекты при постановке эпидурального катетера. В одном случае в результате выраженной деформации позвоночника из-за перелома не удалось четко определить и катетеризировать эпидуральное пространство. Необходимо отметить, что процент осложнений и неудач напрямую связан как с квалификацией анестезиолога, так с появлением новых высокоэффективных и менее токсичных местных анестетиков, совершенствованием техники анестезии и применением специальных одноразовых наборов.
Таким образом, при оператив н ых вмешательствах на позвоночнике и спинном мозге (грыжи межпозвонковых дисков, стенозы позвоночного канала) ЭА является высокоэффективной методикой, способной обеспечить полноценную антистрессовую защиту организма больных при минимальной фармакологической нагрузке. Использование ЭА в послеоперационном периоде создаёт оптимальный анальгетический эффект, способствует ранней активизации больных и дает возможность более быстрого функционального восстановления организма после операции. Методика ЭА при операциях на позвоночнике и спинном мозге имеет гораздо меньше побочных эффектов и осложнений, чем традиционная ОА и должна использоваться значительно чаще. Также следует подчеркнуть, что ЭА особенно предпочтительна у больных пожилого возраста и с высокой степенью операционно-анестезиологического риска.
Литература.
- Соленкова А.В., Лубнин А.Ю., Тенедиева В.Д. и др. Эпидуральная анестезия при оперативных вмешательствах на позвоночнике и спинном мозге. Часть I . Сравнительный анализ адекватности анестезиологической защиты в условиях эпидуральной анестезии и нейролептаналгезии. // Анестезиология и реаниматология. – 2000. – № 4.
- Berkowitz S., Gold M.I. Spinal anesthesia for surgery in patients with previous lumbar laminectomy.// Anest.Analg. -1980. – V.59, p.881-883.
- Calappi E., Parma A., Massei R. Evaluation of plasma levels of catecholamines, prolactin and cortisol during total intravenous anesthesia with propofol in the surgery of the lumbar spine.// Agressologie. – 1994. – V.1, p.43-44.
- Cohen B.E., Hartman M.B., Wade J.T.et all. Postoperative pain control after lumbar spine fusion. Patient-controlled analgesia versus continuous epidural analgesia.// Spine. – 1997. – V.22, p.1892-1896.
- Greenberg P.E., Brown M.D. Epidural anesthesia for lumbar spine surgery. // J.Spin.Disord. – 1988. -V.1, p.139-143.
- Kester K. Epidural pain management for the pediatric spinal fusion patient.// Orthop Nurs. – 1997. – V.16, p.55-60.
- Reynolds A.F., Dautenhahn D.L., Pollay M. Safety and efficacy of epidural analgesia in spine surgery.// Ann. Surg. – 1986. -V. 203, p.225-227.
- Silver D.J., Dunsmore R.H., Dickson C.M. Spinal anesthesia for lumbar disc surgery: review of 576 operations. // Anesth. Analg. – 1976. -V. 55, p. 550-553.
- Wessen A., Peon P.M., Nilsson A. et all. Clinical pharmacokinetics of propofol given as a constant-rate infusion and in combination with epidural blockade. // J. Clin. Anesth. – 1994. – V. 6 , p.193-198.
Регионарная анестезия и лечение боли. Тематический сборник. Москва-Тверь 2004 г., стр.229-238
Источник
